
|
ENZYKLOPÄDIE DER FUNKELEKTRONIK UND ELEKTROTECHNIK Vergleichende Eigenschaften galvanischer Elemente der Größe AA. Enzyklopädie der Funkelektronik und Elektrotechnik
Lexikon der Funkelektronik und Elektrotechnik / Ladegeräte, Batterien, galvanische Zellen Heutzutage findet man in Geschäften und Märkten viele verschiedene galvanische Elemente. Welche soll ich wählen? Dieser Artikel hilft Ihnen, die richtige Entscheidung zu treffen. Galvanische Zellen und Batterien werden häufig zur Stromversorgung verschiedener elektronischer Geräte verwendet. Die gebräuchlichsten Elemente haben die Größe AA. In den Verkaufsregalen finden Sie ähnliche Produkte verschiedener Unternehmen, hauptsächlich aus zwei elektrochemischen Systemen: Kochsalzlösung und Alkali. Vor kurzem begann Energizer mit der Produktion von 1,5-V-Lithiumzellen der Größe AA. Das wichtigste Merkmal einer galvanischen Zelle – die Kapazität (die Strommenge, die sie an eine Last liefern kann) – wird auf dem Etikett fast nie angegeben. Käufer können sich nur auf Fernsehwerbespots über Zellen verlassen, die „bis zu zehnmal länger halten als herkömmliche Salzzellen“, oder sich auf Energizers Wort verlassen, dass seine neuen e2-Lithiumzellen der Größe AA fünfmal länger halten als herkömmliche alkalische Zellen [1]. Darüber hinaus bleibt nicht ganz klar, welche Elemente als „gewöhnlich“ bezeichnet werden. Um die Parameter von Elementen verschiedener elektrochemischer Systeme quantitativ zu vergleichen, ist es notwendig, sie unter den gleichen Bedingungen zu testen. Solche Tests wurden mit drei Arten von Elementen durchgeführt: Salz Philips Long Life (EMF eines „frischen“ Elements – 1,65 V), alkalisches Duracell Ultra MZ (1,62 V) und Lithium Energizer e2 (1,8 V). Jeder von ihnen wurde mit einem 15-Ohm-Widerstand belastet, was einem anfänglichen Entladestrom von etwa 100 mA entspricht. Für Elemente der Standardgröße AA ist dieser Laststrom typisch. Die Entladung erfolgte in Zyklen von mehreren Stunden am Tag, was den realen Betriebsbedingungen entspricht. Dies erklärt die Spannungsspitzen auf den Entladungskurven in Abb. 1. Die blaue Kurve entspricht dem Salzelement, rot dem alkalischen Element und grün dem Lithiumelement. Während der „Ruhe“-Phase stieg die Spannung an einem Element jeglicher Art leicht an, sank jedoch nach dem Anschließen der Last schnell auf das Minimum im vorherigen Zyklus. Die Punkte markieren die Werte der EMF der Elemente – die Spannung an ihnen ohne Last.
Nimmt man als Kriterium für die vollständige Entladung einer Zelle einen Abfall der Spannung an ihrer Last auf 0,9 V, so betrug die experimentell ermittelte Kapazität der Salzzelle 1 Ah, der Alkalizelle 2,9 Ah und der Lithiumzelle 3,5 Ah . Daher besteht keine Notwendigkeit, über fünf- und zehnfache Unterschiede in der Kapazität von Elementen verschiedener elektrochemischer Systeme zu sprechen. Auf Abb. 2 zeigt eine weitere Kurvenserie.
Sie zeigen, wie sich der Innenwiderstand der Elemente während des Entladungsvorgangs verändert. Die Entsprechung zwischen Elementtyp und Kurvenfarbe ist hier die gleiche wie in Abb. 1. Die Werte des Innenwiderstands R wurden nach der Formel berechnet
wobei E die EMF des Elements ist; U - Spannung unter Last; RH ist der Lastwiderstand. Der Innenwiderstand von Salzen und alkalischen Elementen steigt mit fortschreitender Entladung monoton an. Und der Lithiumwiderstand, der zu Beginn der Entladung stark abgenommen hat, bleibt bis zum Schluss praktisch unverändert und steigt dann ebenso stark an. Natürlich können die durchgeführten Experimente nicht als erschöpfend bezeichnet werden. Die Kapazität eines Elements ist kein streng festgelegter Wert, sondern hängt von vielen externen Faktoren ab. Für verschiedene Elemente kann sein Maximum unter deutlich unterschiedlichen Entladebedingungen erreicht werden. Um all dies zu berücksichtigen, müsste eine sehr große Reihe von Experimenten durchgeführt werden, die unter Amateurbedingungen unrealistisch wären. Versuchen wir jedoch, die durch Berechnung erzielten Ergebnisse zu überprüfen. Um die theoretisch maximal mögliche Kapazität von Elementen verschiedener elektrochemischer Systeme abzuschätzen, müssen Sie die chemische Zusammensetzung ihrer Elektroden, des Elektrolyten und die im Element ablaufende chemische Reaktion kennen. Bei Salz- und Alkalizellen besteht die Kathode aus Zink und die Anode aus Mangandioxid. Aus diesem Grund werden solche Elemente zusammenfassend als Mangan-Zink bezeichnet. Der darin enthaltene Elektrolyt ist jedoch ein anderer: Salz (normalerweise Ammoniumchlorid) oder Alkali (Kaliumhydroxid). Nach [2] findet die Reaktion im Element Mangan-Zink-Salz statt
und alkalisch
Über das Elektrodenmaterial und die chemische Reaktion in der Lithiumzelle liegen keine verlässlichen Informationen vor. Man kann nur davon ausgehen, dass die Elektroden aus Lithium und Mangandioxid bestehen und der Elektrolyt eine Lösung von Lithiumperchlorat in Propylencarbonat ist. Wenn diese Vermutung zutrifft, kommt es laut [2] zu einer Reaktion in der Lithiumzelle
Mit dem Faradayschen Gesetz erhalten wir einen Ausdruck zur Bestimmung der Kapazität einer galvanischen Zelle C, Ah:
wobei m die Masse der reagierenden Substanzen ist. F = 96,5–103 C/g-eq – Faraday-Zahl; n - Wertigkeit (für Salz- und alkalische galvanische Zellen - 2, für Lithium - 1); M ist das Gesamtmolekulargewicht der reagierenden Substanzen. Wir wiegen galvanische Zellen der Größe AA: Salz - 17 g, alkalisch - 24 g, Lithium - 15 g. Nehmen wir an, dass im Vergleich zur Masse der reagierenden Stoffe die Masse des Zellkörpers und der nicht beteiligten Stoffe vorhanden sind in der Reaktion (Kohlenstoffelektrode, Elektrolyt in Alkali- und Lithiumzellen) ist vernachlässigbar und kann vernachlässigt werden. Das Gesamtmolekulargewicht der reagierenden Stoffe berechnen wir aus den obigen Gleichungen chemischer Reaktionen: für Salz – 346 g, für Alkali – 257 g, für Lithium – 94 g. Durch Einsetzen von Zahlenwerten in die Formel erhalten wir das maximal mögliche Kapazität der Salzzelle - 2,6 Ah, Alkali - 5 Ah, Lithium - 4,3 Ah. Die Unterschiede zwischen den berechneten und den gemessenen Kapazitätswerten lassen sich durch eher grobe Annahmen bei den Berechnungen erklären. Es wurden also keine fünf- oder zehnfachen Unterschiede festgestellt. Die theoretische Kapazität einer Alkalizelle ist etwa doppelt so groß wie die einer Salzzelle, und Lithium hat in dieser Hinsicht keinen Vorteil gegenüber Alkali. Dies steht im Einklang mit den experimentellen Ergebnissen. Basierend auf den Ergebnissen aller durchgeführten Arbeiten können wir Folgendes schlussfolgern: 1. Lithium-galvanische Zellen haben die stabilste Spannung, den niedrigsten Innenwiderstand, der praktisch nicht vom Grad der Entladung abhängt, und die höchste, wenn auch nicht viel, Kapazität. Sie werden vorzugsweise zur Stromversorgung von Geräten mit hohem Stromverbrauch sowie in Geräten verwendet, die sich bei Abfall der Versorgungsspannung automatisch abschalten (z. B. Digitalkameras). 2. Alkaline-Zellen haben eine mit Lithium vergleichbare Kapazität und sind ebenfalls in der Lage, einen hohen Strom an die Last zu liefern, allerdings bei einer niedrigeren Spannung. Sie kommen am besten in Geräten mit mittlerer Stromaufnahme ohne automatische Spannungsregelung zum Einsatz. In vielen Fällen werden Alkalizellen gegenüber Lithiumzellen bevorzugt, da sie drei- bis viermal günstiger sind. 3. Salzzellen haben die kleinste Kapazität und den höchsten Innenwiderstand. Es empfiehlt sich, sie in Geräten mit geringem Stromverbrauch einzusetzen. Literatur
Autor: I.Podushkin, Moskau
Maschine zum Ausdünnen von Blumen im Garten
02.05.2024 Fortschrittliches Infrarot-Mikroskop
02.05.2024 Luftfalle für Insekten
01.05.2024
▪ Phobos wird vom Mars zerstört ▪ Fledermäuse sind die Hauptüberträger von Viruserkrankungen ▪ Neue Abfallentsorgungstechnologie auf der Internationalen Raumstation ▪ Elektroautos helfen, das Asthmarisiko zu senken
▪ Abschnitt der Website Enzyklopädie der Funkelektronik und Elektrotechnik. Artikelauswahl ▪ Artikel Schiedsrichter der Anmutigen. Populärer Ausdruck ▪ Artikel Was ist ein Asteroid? Ausführliche Antwort ▪ Artikel Organisation eines Büros und einer Ecke des Arbeitsschutzes ▪ Artikel Ersetzen der Karte (sechs Möglichkeiten). Fokusgeheimnis
Kommentare zum Artikel: Gast Erklärender Artikel, danke.
Startseite | Bibliothek | Artikel | Sitemap | Site-Überprüfungen www.diagramm.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






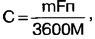
 Hinterlasse deinen Kommentar zu diesem Artikel:
Hinterlasse deinen Kommentar zu diesem Artikel: