
|
Vorlesungsunterlagen, Spickzettel
Krankenhaustherapie. Spickzettel: kurz das Wichtigste
Verzeichnis / Vorlesungsunterlagen, Spickzettel Inhaltsverzeichnis
1. Rheuma. Ätiologie und Pathogenese Rheuma (Sokolsky-Buyo-Krankheit) ist eine systemische entzündliche Erkrankung des Bindegewebes mit überwiegender Lokalisation des Prozesses im Herz-Kreislauf-System, die bei dafür prädisponierten Personen (in der Regel sind dies junge Menschen) aufgrund einer akuten Infektion entsteht mit Gruppe b-hämolytischen Streptokokken ABER. Diese Definition der Krankheit wurde 1989 von V. A. Nasonov gegeben. Die Schädigung anderer Organe und Systeme bei Rheumatismus ist von untergeordneter Bedeutung und bestimmt nicht den Schweregrad und die spätere Prognose. Ätiologie. Beta-hämolysierende Streptokokken der Gruppe A verursachen Infektionen der oberen Atemwege. Aus diesem Grund gehen dem Ausbruch von Rheuma normalerweise Angina pectoris, Exazerbation einer chronischen Tonsillitis und im Blut von Patienten eine erhöhte Menge an Streptokokken-Antigen und Anti-Streptokokken-Antikörpern (ASL-O, ASG, ASA, Antidesoxyribonuklease B (Anti- DNase B)). Bei der Entstehung von Rheuma spielen Alter und soziale Faktoren eine Rolle (ungünstige Lebensbedingungen, Mangelernährung), auch eine genetische Veranlagung (Rheuma ist eine polygene Erbkrankheit, die Existenz „rheumatischer“ Familien ist bekannt), die darin besteht, a Hyperimmunantwort auf Streptococcus-Antigene, die Neigung von Patienten zu Autoimmun- und Immunkomplexprozessen. Pathogenese. Bei Rheuma kommt es zu einer komplexen und vielfältigen Immunantwort (Überempfindlichkeitsreaktionen vom Sofort- und Spättyp) auf zahlreiche Streptokokken-Antigene. Wenn eine Infektion in den Körper eindringt, werden Antistreptokokken-Antikörper produziert und Immunkomplexe gebildet (Streptokokken-Antigene + Antikörper gegen sie + Komplement), die im Blut zirkulieren und sich im Mikrozirkulationsbett absetzen. Auch Streptococcus-Toxine und -Enzyme wirken schädigend auf Myokard und Bindegewebe. Aufgrund eines genetisch bedingten Defekts im Immunsystem werden Streptokokken-Antigene und Immunkomplexe nicht vollständig und schnell aus dem Körper der Patienten eliminiert. Als Ergebnis entwickeln sich Autoimmunprozesse entsprechend der Art der Überempfindlichkeit vom verzögerten Typ, und Lymphozyten, die mit Herzgewebe reagieren, werden im Blut von Patienten gefunden. Diese Zellen sind von großer Bedeutung bei der Entstehung von Organläsionen (hauptsächlich des Herzens). Im Bindegewebe mit Rheuma treten Phasenänderungen auf: Schleimhautschwellung - fibrinoide Veränderungen - fibrinoide Nekrose. Der morphologische Ausdruck von Immunstörungen sind zelluläre Reaktionen - Infiltration durch Lymphozyten und Plasmozyten, die Bildung von rheumatischen oder Ashofftalalaevskaya-Granulomen. Der pathologische Prozess endet mit Sklerose. Wenn das Herz betroffen ist, kann sich der Entzündungsprozess auf alle Membranen des Herzens (Pankarditis) oder isoliert auf jede der Membranen ausbreiten. 2. Klinisches Bild von Rheuma Alle Manifestationen der Krankheit können in kardiale und extrakardiale unterteilt werden. Von diesen Positionen aus kann das Krankheitsbild der Erkrankung beschrieben werden. Stadium I: Der Zusammenhang der Krankheit mit der übertragenen Infektion wird aufgedeckt. In typischen Fällen steigt die Körpertemperatur 1-2 Wochen nach einer Halsentzündung oder einer akuten Atemwegserkrankung an, manchmal bis auf 38-4 ° C, mit Schwankungen im Laufe des Tages innerhalb von 1-2 C und starkem Schweiß (normalerweise ohne Schüttelfrost). Die häufigste Manifestation von Rheuma ist eine Herzschädigung - Rheumatische Herzkrankheit: gleichzeitige Schädigung des Myokards und des Endokards. Patienten klagen über leichte Schmerzen oder Beschwerden in der Herzgegend, leichte Atemnot bei Belastung, Aussetzer oder Herzklopfen sind deutlich seltener. Rheumatische Herzerkrankungen bei jungen Patienten sind in der Regel schwerwiegend: Von Beginn der Erkrankung an werden schwere Atemnot während des Trainings und in Ruhe, ständige Schmerzen im Herzen und Herzklopfen festgestellt. Perikarditis sowie extrakardiale Manifestationen von Rheuma sind selten. Mit der Entwicklung einer trockenen Perikarditis bemerken die Patienten nur ständige Schmerzen im Bereich des Herzens. Bei der exsudativen Perikarditis, die durch die Ansammlung von serös-fibrinösem Exsudat im Herzsack gekennzeichnet ist, verschwindet der Schmerz, da die entzündeten Perikardschichten durch das sich ansammelnde Exsudat getrennt werden. Das charakteristischste Rheuma ist die Niederlage des Bewegungsapparates in Form von rheumatischer Polyarthritis. Rheumatische Läsionen der Nieren sind ebenfalls äußerst selten und werden nur bei der Untersuchung von Urin festgestellt. Das abdominale Syndrom (Peritonitis) tritt fast ausschließlich bei Kindern und Jugendlichen mit akutem primärem Rheumatismus auf. Im Stadium II der diagnostischen Suche ist der Nachweis von Anzeichen einer Herzschädigung von geringer Bedeutung. Bei der primären rheumatischen Herzerkrankung ist das Herz in der Regel nicht vergrößert. Die Auskultation zeigt einen gedämpften I-Ton, manchmal das Auftreten eines III-Tons, ein leises systolisches Geräusch an der Spitze. Diese Symptomatik ist auf Veränderungen im Myokard zurückzuführen. Bei Schäden an der Aortenklappe kann ein protodiastolisches Geräusch am Botkin-Punkt zu hören sein und die Klangfülle des II-Tons erhalten bleiben. Bei Patienten mit Polyarthritis wird eine Gelenkdeformität aufgrund einer Entzündung der Synovialmembran und des periartikulären Gewebes sowie Schmerzen beim Abtasten des Gelenks festgestellt. Ringförmiges Erythem (ein fast pathognomonisches Zeichen für Rheuma) ist äußerst selten (bei 1-2 % der Patienten). In der III. Phase der diagnostischen Suche ermöglichen uns die Daten von Labor- und Instrumentenstudien, die Aktivität des pathologischen Prozesses festzustellen und die Schädigung des Herzens und anderer Organe zu klären. Akute-Phase-Indikatoren: Neutrophilie mit Verschiebung des Leukozytenblutbildes nach links; ein Anstieg des Gehalts an 2-Globulinen, gefolgt von einem Anstieg des Globulinspiegels; erhöhter Fibrinogengehalt; das Auftreten von C-reaktivem Protein; ESR steigt. Immunologische Parameter, erhöhte Titer von Antistreptokokken-Antikörpern (Antihyaluronidase und Antistreptokinase über 1:300, Anti-O-Streptolysin über 1:250). 3. Diagnose von Rheuma Mit dem allmählichen Auftreten von Rheuma ist die von AI Nesterov 1973 vorgeschlagene syndromale Diagnose (siehe Tabelle 1) von Bedeutung: klinisches und epidemiologisches Syndrom; kardiovaskuläres Syndrom (siehe Tabelle 2). Tabelle 1
Tabelle 2
4. Differentialdiagnose von Rheuma Die rheumatische Polyarthritis muss von der nichtrheumatischen abgegrenzt werden (siehe Tabelle). Tabelle
5. Behandlung von Rheuma Der gesamte Komplex der Behandlung von Rheuma besteht aus einer antimikrobiellen und entzündungshemmenden Therapie, Maßnahmen, die auf die Wiederherstellung der immunologischen Homöostase abzielen. Es wird empfohlen, eine rationale, ausgewogene Ernährung zu verwenden, sich auf die Anpassung an körperliche Aktivität, die Vorbereitung auf die Arbeit und die rechtzeitige chirurgische Behandlung von Patienten mit komplexen Herzfehlern zu konzentrieren. Allen Patienten während der aktiven Phase des Rheumatismus wird Penicillin (1-200 IE für 000 Dosen pro Tag alle 1 Stunden) gezeigt, das eine bakterizide Wirkung auf alle Arten von A-Streptokokken hat. Der Behandlungsverlauf beträgt 500 Wochen während der aktiven Rheumaphase, in Zukunft ist eine Umstellung auf das verlängerte Medikament Bicillin-000 (6 Einheiten) erforderlich. Bei Penicillin-Unverträglichkeit kann Erythromycin 4 mg 2-mal täglich verschrieben werden. Medikamente mit entzündungshemmender Wirkung, die in der modernen Behandlung der aktiven Phase von Rheuma eingesetzt werden, sind Glucocorticosteroide, Salicylsäure, Indolderivate, Derivate der Phenylessigsäure usw. Prednisolon wird mit 20-30 mg pro Tag (für 2 Wochen, dann wird die Dosis alle 2,5-5 Tage um 5-7 mg reduziert, insgesamt für einen Zeitraum von 1,5-2 Monaten) für primäre und rezidivierende mit III und II verwendet grad Aktivität des Prozesses der rheumatischen Herzkrankheit, mit Polyserositis und Chorea, mit der Entwicklung von Herzversagen aufgrund aktiver Karditis. Corticoid-Mittel beeinflussen den Wasser-Salz-Stoffwechsel, daher sollten Kaliumchlorid 3-4 g / Tag, Panangin und andere bei der Behandlung mit Flüssigkeitsretention verwendet werden - Aldosteron-Antagonisten (Veroshpiron bis zu 6-8 Tabletten pro Tag), Diuretika (Lasix 40-80 mg / Tag, Furosemid 40-80 mg / Tag usw.), mit Euphorie - Beruhigungsmitteln usw. Nichtsteroidale Antiphlogistika werden auch häufig bei Rheuma eingesetzt: Die durchschnittliche Dosis von Acetylsalicylsäure beträgt 3-4 g pro Tag, seltener 5 g pro Tag oder mehr. Acetylsalicylsäure wird 1 g 3-4 mal täglich nach den Mahlzeiten für 1-3 Monate oder länger bei normaler Verträglichkeit und vorbehaltlich der Kontrolle von Nebenwirkungen verwendet. Die erfolgreiche Anwendung des Indolessigsäure-Derivats - Indomethacin bei Rheuma seit mehr als 20 Jahren. Es hat eine ausgeprägte therapeutische Wirkung: Subjektive Symptome einer Karditis (Herzschmerzen, Herzklopfen, Atemnot) verschwinden am 8.-10. Tag der Therapie und objektive Anzeichen - am 14.-16. Tag. Das Verschwinden von Polyarthritis und Polyserositis erfolgt noch schneller. Bei der Behandlung von Rheuma ist eine Kombination aus drei Hauptstadien wichtig: Krankenhaus – Klinik – Kurort. Im Stadium I wird die Behandlung mit den oben aufgeführten Medikamenten durchgeführt. Nach der Verringerung der Rheumaaktivität und der Normalisierung des Zustands des Patienten werden sie in ein rheumatologisches Sanatorium in die Phase II überführt - Behandlung. Das Hauptziel dieser Phase ist die Fortsetzung der Behandlung mit nichtsteroidalen Antirheumatika. Stadium III umfasst die Beobachtung in der Apotheke und die vorbeugende Behandlung. 6. Klassifikation von Kardiomyopathien. Ätiologie der dilatativen Kardiomyopathie (DCM) Kardiomyopathien sind primär isolierte myokardiale Läsionen nicht entzündlicher Natur unbekannter Ätiologie (idiopathisch), sie sind nicht mit Herzklappenfehlern oder intrakardialen Shunts, arterieller oder pulmonaler Hypertonie, koronarer Herzkrankheit oder systemischen Erkrankungen (wie: Kollagenosen, Amyloidose, Hämochromatose) verbunden , etc.), außerdem entwickeln sich im Endstadium der Erkrankung eine schwere kongestive Herzinsuffizienz und komplexe Verletzungen des Herzrhythmus und der Durchgängigkeit. Die Klassifikation der Kardiomyopathien ist wie folgt: 1) dilatative Kardiomyopathie: a) idiopathisch; b) giftig; c) ansteckend; d) mit Kollagenosen; 2) hypertroph; 3) restriktiv; 4) arrhythmische Dysplasie des rechten Ventrikels; 5) eine Kombination einer der 4 Arten von Kardiomyopathien mit arterieller Hypertonie. Die dilatative Kardiomyopathie (DCM) ist eine Erkrankung des Herzmuskels, die durch eine diffuse Erweiterung aller Herzkammern (hauptsächlich des linken Ventrikels) gekennzeichnet ist, bei der die Pathologie der Pumpfunktion des Herzens im Vordergrund steht und als Folge davon , chronische Herzinsuffizienz (daher der zweite Name kongestiv, wenn das Herz das Blut nicht vollständig pumpen kann und es in den Geweben und Organen des Körpers "stagniert"). Die Muskelwand des Herzens bleibt entweder unverändert oder in unterschiedlichem Maße hypertrophiert. Krankheiten und Faktoren, die der Entwicklung von DCMP vorausgingen, sind in der folgenden Tabelle beschrieben (siehe Tabelle). Tisch. Krankheiten und Faktoren, die der Entwicklung von DCM vorausgingen
Dies ist die häufigste Form der Schädigung des Herzmuskels. Die Inzidenz beträgt 5-8 Fälle pro 100 Einwohner pro Jahr. Für diese Patienten gibt es keine eindeutige Familienanamnese. Männer erkranken 000-2 Mal häufiger als Frauen. 7. Pathogenese der dilatativen Kardiomyopathie (DCM) Pathogenese. Als Folge des Entzündungsprozesses im Herzmuskel (Myokarditis) sterben einzelne Zellen in seinen verschiedenen Teilen ab. Die Entzündung ist in diesem Fall viraler Natur, und die vom Virus betroffenen Zellen werden zu Fremdstoffen für den Körper. Wenn Antigene im Körper auftreten, entwickelt sich dementsprechend ein Komplex von Immunreaktionen, die auf ihre Zerstörung abzielen. Allmählich werden die toten Muskelzellen durch Bindegewebe ersetzt, das nicht die dem Myokard innewohnende Fähigkeit zur Dehnbarkeit und Kontraktilität besitzt. Durch den Verlust der Hauptfunktionen des Myokards verliert das Herz seine Funktion als Pumpe. Als Reaktion darauf (als kompensatorische Reaktion) dehnen sich die Herzkammern aus (d. h. sie dehnen sich aus), und es kommt zu einer Verdickung und Verdickung im verbleibenden Teil des Myokards (d. h. seine Hypertrophie entwickelt sich). Um die Sauerstoffzufuhr zu den Organen und Geweben des Körpers zu erhöhen, tritt eine anhaltende Erhöhung der Herzfrequenz (Sinustachykardie) auf. Diese kompensatorische Reaktion verbessert nur vorübergehend die Pumpfunktion des Herzens. Die Möglichkeiten der myokardialen Dilatation und Hypertrophie sind jedoch durch die Menge an lebensfähigem Myokard begrenzt und für jeden spezifischen Krankheitsfall individuell. Mit dem Übergang des Prozesses in das Stadium der Dekompensation entwickelt sich eine chronische Herzinsuffizienz. Allerdings kommt in diesem Stadium ein weiterer Ausgleichsmechanismus ins Spiel: Das Gewebe des Körpers erhöht die Entnahme von Sauerstoff aus dem Blut im Vergleich zu einem gesunden Körper. Dieser Mechanismus ist jedoch unzureichend, da eine Abnahme der Pumpfunktion des Herzens zu einer Abnahme der Sauerstoffversorgung von Organen und Geweben führt, die für ihre normale Funktion erforderlich ist, während die Menge an Kohlendioxid in ihnen zunimmt. Bei 2/3 der Patienten in den Hohlräumen der Ventrikel bilden sich im Spätstadium der Erkrankung parietale Thromben (aufgrund einer Abnahme der Pumpfunktion des Herzens sowie einer ungleichmäßigen Kontraktion des Myokards in den Herzkammern). ), gefolgt von der Entwicklung einer Embolie im Lungen- oder Körperkreislauf. Pathohistologische und pathomorphologische Veränderungen im Herzen. Die Form des Herzens wird kugelförmig, seine Masse steigt von 500 auf 1000 g, hauptsächlich aufgrund des linken Ventrikels. Das Myokard wird schlaff, stumpf, mit auffälligen weißlichen Bindegewebsschichten, es gibt einen charakteristischen Wechsel von hypertrophen und atrophischen Kardiomyozyten. Mikroskopisch wird eine diffuse Fibrose nachgewiesen, die sowohl mit Atrophie als auch mit Hypertrophie von Kardiomyozyten kombiniert werden kann, bei der das Volumen der Kerne, die Anzahl der Mitochondrien, die Hyperplasie des Golgi-Apparats und die Anzahl der Myofibrillen signifikant ansteigen , frei und mit den Ribosomen des endoplasmatischen Retikulums verbunden, eine Fülle von Glykogenkörnchen. 8. Klinisches Bild und Diagnose Dilatative Kardiomyopathie (DCM) Es gibt keine spezifischen Anzeichen der Krankheit. Das Krankheitsbild ist polymorph und wird bestimmt durch: 1) Symptome einer Herzinsuffizienz; 2) Rhythmus- und Leitungsstörungen; 3) thromboembolisches Syndrom. In den meisten Fällen wird die Prognose der Krankheit durch die Niederlage der linken Herzkammer bestimmt. Vor dem Einsetzen einer Herzinsuffizienz ist DCM latent. Die häufigsten Beschwerden einer bereits einsetzenden Herzinsuffizienz sind Beschwerden über verminderte Leistungsfähigkeit, erhöhte Müdigkeit, Atemnot bei Belastung und dann in Ruhe. Nachts hat er einen trockenen Husten (das Äquivalent von Herzasthma), später - typische Asthmaanfälle. Die Patienten stellen sich mit charakteristischen Angina-Schmerzen vor. Mit der Entwicklung einer Stauung im systemischen Kreislauf tritt Schweregefühl im rechten Hypochondrium auf (aufgrund einer vergrößerten Leber), Schwellung der Beine. Diagnose. Bei der Diagnose der Krankheit ist ein wichtiges Zeichen ein signifikanter Anstieg des Herzens (es gibt keine Anzeichen einer Herzklappenerkrankung oder einer arteriellen Hypertonie). Die Kardiomegalie äußert sich durch die perkussionsbedingte Ausdehnung des Herzens in beide Richtungen sowie die Verschiebung des Spitzenschlags nach links und unten. In schweren Fällen sind ein Galopprhythmus, Tachykardie, Geräusche einer relativen Insuffizienz der Mitral- oder Trikuspidalklappen zu hören. In 20 % der Fälle entwickelt sich Vorhofflimmern. Der Blutdruck ist normalerweise normal oder leicht erhöht (aufgrund einer Herzinsuffizienz). Biochemische Untersuchungen von Blut und Urin können verschiedene toxische Substanzen sowie Vitaminmangel nachweisen. Instrumentelle Forschungsmethoden ermöglichen den Nachweis von: 1) Anzeichen von Kardiomegalie; 2) die Veränderungen in den Kennziffern der zentralen Hämodynamik; 3) Rhythmus- und Leitungsstörungen. Das Phonokardiogramm bestätigt auskultatorische Daten in Form eines Galopprhythmus, ein ziemlich häufiger Nachweis eines systolischen Geräuschs. Röntgenaufnahmen zeigen eine signifikante Zunahme der Ventrikel und eine Stagnation des Blutes im Lungenkreislauf (kleinen Kreislauf). Die Echokardiographie hilft, eine Dilatation beider Ventrikel, eine Hypokinesie der hinteren Wand des linken Ventrikels und eine paradoxe Bewegung des interventrikulären Septums während der Systole zu erkennen. Eine Radioisotopenuntersuchung des Herzens (Myokardszintigraphie) wird durchgeführt, um den Zustand der Pumpfunktion des Herzens zu klären und die Zonen des toten Myokards zu bestimmen. Angiokardiographisch werden die gleichen Veränderungen wie im Echokardiogramm festgestellt. Eine Live-Myokardbiopsie ist nicht aussagekräftig für die Bestimmung der Ätiologie der Kardiomyopathie. In einigen Fällen kann in der Biopsie ein virales Antigen oder ein Anstieg des LDH-Gehalts sowie eine Abnahme der Energieproduktion durch Mitochondrien nachgewiesen werden. 9. Differenzialdiagnose / Dilatative Kardiomyopathie (DCM) Es wird hauptsächlich bei Myokarditis und myokardialen Dystrophien produziert, d.h. bei solchen Zuständen, die manchmal zu Unrecht als sekundäre Kardiomyopathien bezeichnet werden. Eine Myokardbiopsie leistet eine wichtige Hilfestellung bei der Differentialdiagnose einer dilatativen Kardiomyopathie und einer Herzerkrankung, die mit einer ausgeprägten Zunahme derselben auftritt: 1) bei schwerer diffuser Myokarditis findet sich eine zelluläre Infiltration des Stromas in Kombination mit dystrophischen und nekrotischen Veränderungen in Kardiomyozyten; 2) bei primärer Amyloidose, die mit Herzschäden auftritt (die sogenannte kardiopathische Variante der primären Amyloidose), kommt es zu einer signifikanten Ablagerung von Amyloid im interstitiellen Gewebe des Myokards, verbunden mit einer Atrophie von Muskelfasern; 3) Bei Hämochromatose (einer Krankheit, die durch eine Verletzung des Eisenstoffwechsels verursacht wird) werden Ablagerungen von eisenhaltigem Pigment im Myokard gefunden, verschiedene Grade von Dystrophie und Atrophie von Muskelfasern und eine Proliferation von Bindegewebe werden beobachtet. Als Variante der DCM kommen medikamenteninduzierte und toxische Kardiomyopathien in Betracht. Многочисленные агенты могут вызвать токсические повреждения миокарда: этанол, эметин, литий, кадмий, кобальт, мышьяк, изпротеренол и другие яды. Патогистологические изменения в тканях сердечной мышцы проявляются в виде очаговых дистрофий. Самым ярким примером токсической кардиомиопатии является кардиомиопатия, которая наблюдается у людей, избыточно потребляющих пиво. В острой стадии течения кобальтовой кардиомиопатии отмечаются наличие гидропической и жировой дистрофии, деструкция внутриклеточных органелл, очаговый некроз кардиомиоцитов. Alkoholische Kardiomyopathie. Ethanol hat eine direkte toxische Wirkung auf Kardiomyozyten. Makroskopisch ist das Myokard schlaff, lehmartig, manchmal werden kleine Narben beobachtet. Die Koronararterien sind intakt. Die mikroskopische Untersuchung zeigt eine Kombination aus Dystrophie (hydropisch und fettig), Atrophie und Hypertrophie von Kardiomyozyten, möglicherweise das Vorhandensein von Herden von Kardiomyozytenlyse und Sklerose. Die betroffenen Bereiche des Myokards kontrastieren mit unveränderten. Die elektronenmikroskopische Untersuchung von Herzbiopsieproben zeigt eine zystische Expansion des sarkoplasmatischen Retikulums und des T-Systems der Kardiomyozyten, was charakteristisch für die alkoholische Kardiomyopathie ist. Komplikationen der alkoholischen Kardiomyopathie - plötzlicher Tod infolge von Kammerflimmern oder chronischer Herzinsuffizienz, thromboembolisches Syndrom. 10. Behandlung und Vorbeugung der dilatativen Kardiomyopathie (DCM) Die allgemeinen Prinzipien für die Behandlung von DCM unterscheiden sich nicht wesentlich von der Behandlung von chronischer Herzinsuffizienz. Bei sekundärer DCM wird zusätzlich die Behandlung der Vorerkrankung (Herzklappenerkrankung etc.) durchgeführt und alle Maßnahmen ergriffen, um die Ursachen der DCM zu beseitigen. Periphere Vasodilatatoren sind sehr effektiv, insbesondere bei gleichzeitigem Angina-Syndrom (Nitrong, Sustak, Nitrosorbid). Beim Angina-Syndrom wird es notwendig, antianginöse Medikamente zu verwenden, vorzugsweise verlängerte Nitrate (Sustak, Nitrong, Nitrosorbid). Adrenoblocker sind wirksam (sie werden verschrieben, wenn keine Anzeichen einer Herzinsuffizienz vorliegen). Von den modernen Methoden der chirurgischen Behandlung von DCMP ist die Herztransplantation (Transplantation) die effektivste. Die Möglichkeiten zur Durchführung dieser Operation sind jedoch erheblich eingeschränkt. Aus diesem Grund wurden als Alternative zur Herztransplantation in der modernen Behandlung zur Erhöhung der Lebenserwartung von Patienten mit DCM rekonstruktive Operationen entwickelt und durchgeführt, die darauf abzielen, die Insuffizienz der Mitral- und Trikuspidalklappen zu beseitigen. Eine Alternative zur Herztransplantation bei Patienten mit DCM ist die teilweise Entfernung der linken Herzkammer, um sie zu verkleinern (Baptiste-Operation). Vor nicht allzu langer Zeit wurden für die Behandlung von Patienten mit DCMP spezielle Schrittmachermodelle entwickelt, mit denen Sie die Arbeit der Herzkammern synchronisieren können. Dies führt zu einer Verbesserung der Füllung der Herzkammern mit Blut und einer Steigerung der Pumpfunktion des Herzens. DCM bei Kindern beträgt 5-10 Fälle pro 100 Kinder pro Jahr. Die größte Wirkung bei der Behandlung der dilatativen Kardiomyopathie bei Kleinkindern wird mit einer Kombination aus Kortikosteroiden und Glykosiden (Prednisolon und Digoxin) erzielt. Vor dem Hintergrund der Monotherapie mit Prednisolon kommt es zu einer Abnahme der Herzfrequenz. Eine Monotherapie mit Digoxin führt zu einer Abnahme von Tachykardie und Dyspnoe. Angesichts der Unratsamkeit der Verschreibung von Zytostatika bei kleinen Kindern, da eine signifikante Anzahl von Behandlungskomplikationen beobachtet wurde, ist es in der Pädiatrie optimaler, langwirksame Herzglykoside in Kombination mit Kortikosteroidhormonen bei dilatativer Kardiomyopathie einzusetzen. Verhütung. Die Prävention von DCMP besteht im Ausschluss von Alkohol, Kokain sowie einer sorgfältigen Überwachung der Herzleistung während der Tumor-Chemotherapie. Es ist nützlich, den Körper von klein auf zu härten. Die vollständige Abstinenz von Alkohol bei alkoholischer DCM verbessert die Kontraktilität des Herzens und kann die Notwendigkeit einer Herztransplantation beseitigen. 11. Klassifikation von Kardiomyopathien. Ätiologie der hypertrophen Kardiomyopathie (HCM) Die hypertrophe Kardiomyopathie (HCM) ist eine nicht koronare Erkrankung des ventrikulären Myokards (hauptsächlich des linken), gekennzeichnet durch eine massive Hypertrophie ihrer Wände mit Vorwölbung des interventrikulären Septums (IVS) in den Hohlraum des rechten Ventrikels, der erheblich verdickt sein kann , eine Abnahme des Innenvolumens der Ventrikel, eine normale oder erhöhte Kontraktilität des ventrikulären Myokards und eine beeinträchtigte Entspannung (diastolische Dysfunktion). Am häufigsten ist eine isolierte Hypertrophie des interventrikulären Septums (isolierte hypertrophe Subaortenstenose - IHSS) oder des apikalen Teils der Ventrikel. Einstufung. Klassifikation der HCM durch Lokalisation der Hypertrophie (ED Wigle et al., 1985 mit Ergänzungen). I. LV-Hypertrophie. 1. Asymmetrische Hypertrophie, bei der Myokardhypertrophie einzelner Wände oder Segmente der Ventrikel auftritt (einschließlich IVS-Hypertrophie - 90% mit oder ohne Obstruktion des linksventrikulären Ausflusstrakts, Mittelkammer - 1%, apikale linksventrikuläre Hypertrophie - 3%, Hypertrophie der freien Wand). linker Ventrikel und hinterer Teil des IVS - 1%). 2. Symmetrische (konzentrische) Hypertrophie des linken Ventrikels, wenn sich die Myokardhypertrophie auf alle Wände der Ventrikel erstreckt, tritt in 5% der Fälle auf. II. Hypertrophie der Bauchspeicheldrüse. Wenn die Myokardhypertrophie den normalen Blutabfluss aus den Herzkammern verhindert, spricht man von einer obstruktiven Form der HCM. In anderen Fällen ist HCM nicht obstruktiv. Ätiologie. Die Krankheit kann entweder angeboren oder erworben sein. Die angeborene HCM wird autosomal-dominant vererbt. Innerhalb derselben Familie können verschiedene Formen und Varianten von HCM beobachtet werden. Am häufigsten wird eine asymmetrische Hypertrophie des interventrikulären Septums vererbt. Die erworbene Form der HCM tritt bei älteren Patienten mit arterieller Hypertonie in der Vorgeschichte auf. Die Prävalenz beträgt 0,02-0,05 %. Die Gründe für die Entwicklung erworbener HCM sind nicht vollständig geklärt. Gemäß einer der vorgeschlagenen Hypothesen entwickeln Personen mit erworbener HCM in der pränatalen Phase einen Defekt in den adrenergen Rezeptoren des Herzens, die an der Regulation der Herzaktivität, insbesondere der Herzfrequenz, beteiligt sind. Infolgedessen wird die Empfindlichkeit gegenüber Noradrenalin und ähnlichen Hormonen, die die Herzfrequenz erhöhen, deutlich erhöht, was die Entwicklung einer Myokardhypertrophie bei ihnen und schließlich HCM beeinflusst. pathologisches Bild. Desorientierte, unregelmäßige, chaotische Anordnung von Kardiomyozyten und Myofibrillen in Kardiomyozyten, Myokardfibrose ist eine Verletzung der Architektur des Herzmuskels. 12. Klinisches Bild und Diagnose einer hypertrophen Kardiomyopathie (HCM) Krankheitsbild. HCM zeichnet sich durch eine extreme Vielfalt an Symptomen aus, die die Ursache für Fehldiagnosen ist. Das Vorhandensein und der Zeitpunkt des Auftretens von Beschwerden bei HCM werden hauptsächlich von 2 Faktoren bestimmt: der Form von HCM und der Lokalisation der Läsion. Die stärkste Kammer des Herzens ist der linke Ventrikel, daher können bei Hypertrophie des Myokards seiner Wände Beschwerden nicht lange auftreten. Die isolierte Infektion der rechten Herzkammer trifft sich äußerst selten. Das Krankheitsbild der HCM ist: 1) Anzeichen einer ventrikulären Myokardhypertrophie (hauptsächlich links); 2) ein Zeichen einer unzureichenden diastolischen Ventrikelfunktion; 3) variable Anzeichen einer Obstruktion des linksventrikulären Ausflusstrakts. Diagnose. Im Prozess der diagnostischen Suche ist die Erkennung eines systolischen Geräuschs, eines veränderten Pulses und eines verschobenen Spitzenschlags am wichtigsten. Für die Diagnose von HCM sind Echokardiographiedaten von größter Bedeutung, um die anatomischen Merkmale der Erkrankung, den Schweregrad der Myokardhypertrophie und die Obstruktion des Ausflusstrakts des linken Ventrikels zu klären. Die folgenden Anzeichen zeigen sich: asymmetrische Hypertrophie des IVS, ausgeprägter im oberen Drittel, seine Hypokinese; systolische Bewegung des vorderen Mitralklappensegels in anteriorer Richtung; Kontakt des vorderen Mitralklappensegels mit dem IVS in der Diastole. Unspezifische Anzeichen sind: Hypertrophie des linken Vorhofs, Hypertrophie der hinteren Wand des linken Ventrikels, eine Abnahme der durchschnittlichen Geschwindigkeit der diastolischen Abdeckung des vorderen Mitralklappensegels. Im EKG finden sich spezifische Veränderungen nur bei ausreichend ausgeprägter linksventrikulärer Hypertrophie. Die Röntgendiagnostik ist nur im fortgeschrittenen Stadium der Erkrankung wichtig, wenn eine Vergrößerung des linken Ventrikels und des linken Vorhofs, eine Erweiterung des absteigenden Teils der Aorta festgestellt werden kann. Auf dem Phonokardiogramm bleiben die Amplituden der Töne I und II erhalten, was ein differenzielles Zeichen der HCM von der Stenose der Aortenöffnung ist, und es wird auch ein systolisches Geräusch unterschiedlicher Schwere festgestellt. Invasive Untersuchungsmethoden (Sondierung des linken Herzens, Kontrastangiographie) sind derzeit nicht zwingend erforderlich, da die Echokardiographie recht zuverlässige Informationen für die Diagnosestellung liefert. Die Herzsondierung wird unter Röntgenfernsehkontrolle verwendet. Technik zur Durchführung des Verfahrens: Durch Punktion einer großen Arterie unter örtlicher Betäubung mit weiterem Einführen eines speziellen Katheters in die Herzhöhle wird der Druckgradient (Differenz) zwischen der linken Herzkammer und der abgehenden Aorta gemessen. Normalerweise sollte dieser Gradient nicht sein. 13. Behandlung und Prävention der hypertrophen Kardiomyopathie (HCM) Behandlung. Grundlage der medikamentösen Behandlung der HCM sind Medikamente, die die Blutversorgung der Herzkammern in der Diastole verbessern. Diese Medikamente sind eine Gruppe von B-Blockern (Anaprilin, Atenolol, Metoprolol und Propranolol, 160-320 mg / Tag usw.) und eine Gruppe von Calciumionenantagonisten (Verapamil, aber mit Vorsicht). Novokinamid-Disopyramid senkt auch die Herzfrequenz und wirkt antiarrhythmisch. Zu Beginn der Behandlung werden kleine Dosen dieser Medikamente verwendet, dann erfolgt eine allmähliche Erhöhung der Dosierung auf das vom Patienten tolerierte Maximum. Bei Diabetes mellitus, Asthma bronchiale und einigen anderen Erkrankungen werden β-Blocker mit Vorsicht eingesetzt. Bei der Behandlung mit diesen Medikamenten ist eine ständige Überwachung des Blutdrucks und der Pulsfrequenz erforderlich. Ein Druckabfall unter 90/60 mm Hg ist gefährlich. Kunst. und Herzfrequenz unter 55 pro Minute. Wenn ein Patient gefährliche Rhythmusstörungen hat, die nicht mit B-Blockern oder Kalziumionenantagonisten behandelt werden können, werden bei der Behandlung dieser Patienten zusätzlich andere Antiarrhythmika eingesetzt. Die Ernennung von Antikoagulanzien wird bei paroxysmalen Arrhythmien und Vorhofflimmern sowie bei Vorhandensein von Blutgerinnseln in den Herzkammern (Warfarin usw.) empfohlen. Während der Behandlung mit diesen Medikamenten müssen regelmäßig eine Reihe von Indikatoren des Blutgerinnungssystems überwacht werden. Bei einer erheblichen Überdosierung von Antikoagulanzien sind äußere (nasale, uterine usw.) und innere Blutungen (Hämatome usw.) möglich. Eine chirurgische Behandlung wird bei Patienten mit obstruktiver HCM durchgeführt, wenn die medizinische Behandlung nicht wirksam ist oder wenn der Gradient zwischen dem linken Ventrikel und der Aorta mehr als 30 mm Hg beträgt. Kunst. (Die Operation der Myotomie oder Myektomie wird durchgeführt - Exzision oder Entfernung eines Teils des hypertrophierten Myokards des linken Ventrikels). Ein Mitralklappenersatz und eine nicht-chirurgische IVS-Ablation werden ebenfalls durchgeführt. Verhütung. Alle Patienten mit HCM, insbesondere solche mit obstruktiver Form, sind bei Sportarten kontraindiziert, bei denen eine starke Steigerung der körperlichen Aktivität in kurzer Zeit möglich ist (Leichtathletik, Fußball, Hockey). Die Vorbeugung der Krankheit besteht in einer frühen Diagnose, die es ermöglicht, früh mit der Behandlung der Krankheit zu beginnen und die Entwicklung einer schweren Myokardhypertrophie zu verhindern. Bei den genetischen Verwandten des Patienten sollte ein Echokardiogramm durchgeführt werden. Wichtig für die Diagnostik sind auch Screening-EKG und EchoCG, die im Rahmen der jährlichen ärztlichen Untersuchung durchgeführt werden. Bei Patienten mit obstruktiver HCM sollte eine Prophylaxe einer infektiösen Endokarditis (Antibiotikaprophylaxe etc.) durchgeführt werden, da das Vorliegen einer Obstruktion die Voraussetzungen für die Entwicklung dieses lebensbedrohlichen Zustands schafft. 14. Ursachen der restriktiven Kardiomyopathie (RCMP) Restriktive Kardiomyopathie (RCMP) - (vom lateinischen Wort "restrictio" - "Einschränkung") - eine Gruppe von Erkrankungen des Myokards und Endokards, bei denen infolge ausgeprägter Fibrose und Elastizitätsverlust aus verschiedenen Gründen eine Fixierung vorliegt Einschränkung der Ventrikelfüllung in der Diastole. RCMP umfasst: Leflers parietale fibroplastische Endokarditis (gefunden in Ländern mit gemäßigtem Klima, beschrieben von W. Loffler et al., 1936) und Endomyokardfibrose (gefunden in Ländern des tropischen Afrikas, beschrieben von D. Bedford et E. Konstman). Причины возникновения РКМП. Первичная РКМП встречается очень редко, и единственной доказанной причиной ее возникновения является так называемый гиперэозинофильный синдром (болезнь Леффлера, лефлеровский париетальный фибропластический эндокардит). Встречается преимущественно у мужчин в возрасте 30-40 лет. При гиперэозинофильном синдроме происходит воспаление эндокарда, со временем завершающееся значительным уплотнением эндокарда и грубым его спаянием с рядом расположенным миокардом, что ведет к резкому снижению растяжимости сердечной мышцы. Для лефлеровского синдрома также характерны персистирующая на протяжении 6 месяцев и более эозинофиллия (1500 эозинофиллов в 1 мм3), поражение внутренних органов (печени, почек, легких, костного мозга). In der überwiegenden Mehrheit der Fälle ist der Ursprung von RCMP aus anderen Gründen sekundär, von denen die häufigsten sind: 1) Amyloidose - eine Krankheit, die mit einer Verletzung des Proteinstoffwechsels im Körper verbunden ist; gleichzeitig wird in den Geweben verschiedener Organe ein abnormales Protein (Amyloid) gebildet und in großen Mengen abgelagert; wenn das Herz geschädigt ist, verursacht Amyloid eine Abnahme seiner Kontraktilität und Dehnbarkeit; 2) Hämochromatose - eine Verletzung des Eisenstoffwechsels im Körper, begleitet von einem erhöhten Eisengehalt im Blut, dessen Überschuss in vielen Organen und Geweben, einschließlich des Myokards, abgelagert wird, wodurch seine Dehnbarkeit abnimmt; 3) Sarkoidose - eine Krankheit unbekannter Ätiologie, gekennzeichnet durch die Bildung von Zellhaufen (Granulomen) in Organen und Geweben; am häufigsten sind Lunge, Leber, Lymphknoten und Milz betroffen; und sich entwickelnde Granulome im Myokard führen zu einer Abnahme seiner Dehnbarkeit; 4) Endokarderkrankungen (Endokardfibrose, Endokardfibroelastose usw.), wenn es zu einer signifikanten Verdickung und Verdichtung des Endokards kommt, was auch zu einer starken Einschränkung der myokardialen Dehnbarkeit führt. Insbesondere die Fibroelastose des Endokards kann nur bei Säuglingen auftreten; Diese Krankheit ist aufgrund der frühen Entwicklung einer schweren Herzinsuffizienz nicht mit dem Leben vereinbar. 15. Klinisches Bild und Diagnose der restriktiven Kardiomyopathie (RCMP) Krankheitsbild. Die Manifestationen der Krankheit sind äußerst polymorph und werden durch die Symptome von Durchblutungsstörungen im kleinen oder großen Kreis (je nach vorherrschender Läsion der rechten oder linken Herzkammer) bestimmt. Beschwerden können ausbleiben oder auf eine Stauung im Lungen- oder Körperkreislauf zurückzuführen sein. Die Patienten klagen in der Regel über Kurzatmigkeit, die zuerst bei körperlicher Anstrengung auftritt, und im weiteren Verlauf der Krankheit wird Kurzatmigkeit in Ruhe beobachtet. Aufgrund einer Abnahme der Pumpfunktion des Herzens klagt der Patient über Müdigkeit und schlechte Belastungstoleranz. Mit der Zeit kommen Schwellungen der Beine, eine vergrößerte Leber und Bauchwassersucht hinzu. In regelmäßigen Abständen tritt ein unregelmäßiger Herzschlag auf, und mit der Entwicklung anhaltender Blockaden kann es zu Ohnmachtsanfällen kommen. Das erste Stadium der Entwicklung der Krankheit (nekrotisch) ist durch das Auftreten von Fieber, Gewichtsverlust, Husten, Hautausschlag und Tachykardie gekennzeichnet. Diagnose. Die Anerkennung von RCM ist äußerst schwierig. Über diese Pathologie kann erst nach Ausschluss einer Reihe ähnlich auftretender Erkrankungen (wie idiopathische Myokarditis vom Abramov-Fiedler-Typ, exsudative Perikarditis, Herzklappenerkrankung) mit Zuversicht gesprochen werden. Bei der Untersuchung von Patienten mit RCMP werden Symptome gefunden, die für kongestive Herzinsuffizienz (Ödeme, Hepatomegalie und Aszites) charakteristisch sind, sowie ein ausgeprägtes Pulsieren der Halsvenen. Bei der Auskultation ist die Erkennung eines vergrößerten Herzens, eines leisen spätsystolischen Geräuschs und eines lauten frühen III-Tons von großer Bedeutung. Eine EKG-Untersuchung zeigt eine mäßige Hypertrophie des ventrikulären Myokards sowie verschiedene Rhythmus- und Leitungsstörungen des Herzimpulses, unspezifische Veränderungen der T-Welle im EKG. Die Echokardiographie ist eine der informativsten Methoden zur Diagnose der Krankheit, mit deren Hilfe eine Verdickung des Endokards, eine Veränderung der Füllung der Herzkammern, eine Abnahme der Pumpfunktion des Herzens, eine schnelle Bewegung des vorderen Segels der Mitralklappe während der Diastole und eine schnelle frühe Bewegung der hinteren Wand des linken Ventrikels nach außen festgestellt werden. Mit der Magnetresonanztomographie können Sie Informationen über die Anatomie des Herzens gewinnen, pathologische Einschlüsse im Myokard bestimmen und die Dicke des Endokards messen. Bei der Untersuchung der Parameter der zentralen Hämodynamik wird ein erhöhter Füllungsdruck in beiden Ventrikeln festgestellt, wobei der Enddruck im linken den im rechten Ventrikel übersteigt. Die Ventrikulographie zeigt eine erhöhte Kontraktion des linken Ventrikels, glatte Konturen seiner Wände, manchmal mit einem Füllungsdefekt in der Spitze (Hinweis auf Obliteration). Es gibt Anzeichen einer Herzklappeninsuffizienz, insbesondere der Mitral- oder Trikuspidalklappe. 16. Differentialdiagnose, Behandlung und Prävention der restriktiven Kardiomyopathie (RCMP) Differenzialdiagnose. Bei der Differentialdiagnose von RCMP ist es sehr wichtig, die Ähnlichkeit der Krankheit bei äußeren Manifestationen mit konstriktiver Perikarditis zu berücksichtigen, aber die Behandlungsmethode für diese Krankheiten ist diametral entgegengesetzt. Die Live-Biopsie des Myokards und des Endokards wird normalerweise gleichzeitig mit der Herzsondierung durchgeführt, wodurch Sie mehr Informationen erhalten, um die Art der Krankheit und die weitere Behandlung zu klären. In extrem seltenen Fällen, wenn die oben genannten diagnostischen Methoden keine Unterscheidung zwischen RCMP und konstriktiver Perikarditis zulassen, wird eine direkte Revision des Perikards auf dem Operationstisch durchgeführt. Alle Patienten mit RCMP benötigen eine umfassende klinische, biochemische und zusätzliche Untersuchung, um nicht-kardiale Ursachen der Erkrankung zu bestimmen. Behandlung. Die Behandlung der Krankheit bereitet erhebliche Schwierigkeiten. Die meisten Medikamente, die zur Behandlung von Herzinsuffizienz eingesetzt werden, bringen möglicherweise nicht die gewünschten Ergebnisse, da es aufgrund der Art der Erkrankung unmöglich ist, eine signifikante Verbesserung der myokardialen Compliance zu erzielen (in einigen Fällen werden Calciumionenantagonisten verschrieben). für diesen Zweck). Diuretika (Aldactone) werden verwendet, um überschüssige Flüssigkeit im Körper auszuscheiden. Um anhaltende Überleitungsstörungen zu beseitigen, kann es notwendig sein, einen dauerhaften Herzschrittmacher einzurichten (implantieren). Dies wird durch Krankheiten wie Sarkoidose und Hämochromatose verursacht, die zur Entwicklung von sekundärem RCMP führen und einer Selbstbehandlung unterliegen. Bei der Behandlung von Sarkoidose werden hormonelle Medikamente (Prednisolon usw.) und bei Hämochromatose regelmäßig Aderlass (um die Eisenkonzentration im Körper zu reduzieren) verwendet. Die Behandlung der myokardialen Amyloidose hängt direkt von den Ursachen ihres Auftretens ab. Es ist ratsam, gerinnungshemmende Medikamente gegen Thrombosen in den Herzkammern zu verwenden. In Fällen von RCMP, die durch eine Endokardschädigung verursacht werden, wird auf eine chirurgische Behandlung zurückgegriffen. Während der Operation wird nach Möglichkeit der veränderte Teil des Endokards entfernt. In einigen Fällen wird bei Insuffizienz der atrioventrikulären Klappen deren Prothese durchgeführt. Einige Formen der amyloiden Myokardschädigung werden mit einer Herztransplantation behandelt. Prävention von RCM. Leider sind vorbeugende Maßnahmen für diese Krankheit begrenzt. Notwendig ist vor allem die Früherkennung potenziell behebbarer Ursachen für Amyloidose, Sarkoidose, Hämochromatose etc. Um diese Ziele zu erreichen, sind jährliche ärztliche Untersuchungen der Bevölkerung von großer Bedeutung. 17. Ätiologie der infektiösen Endokarditis (IE) Infektiöse Endokarditis (IE) ist eine Krankheit, die in einer polyposis-ulzerativen Läsion des Herzklappenapparates (oft mit der Entwicklung einer Klappeninsuffizienz) oder des parietalen Endokards (seltener ist das Endothel der Aorta oder der nächsten großen Arterie betroffen) besteht ). Die Krankheit wird durch verschiedene pathogene Mikroorganismen verursacht und geht mit einer systemischen Läsion der inneren Organe (Nieren, Leber, Milz) vor dem Hintergrund einer veränderten Reaktivität des Körpers einher. Ätiologie. Die pathogenen Erreger der Krankheit sind am häufigsten die Kokkengruppe der Mikroorganismen - Streptokokken (Viridans-Streptokokken wurden zuvor in 90 % der Fälle isoliert), Staphylokokken (golden, weiß), Enterokokken, Pneumokokken. Durch den weit verbreiteten Einsatz von Antibiotika hat sich in den letzten Jahren das Spektrum mikrobieller Krankheitserreger verändert. Die Krankheit kann durch gramnegative Flora (Escherichia coli, Pseudomonas aeruginosa, Proteus, Klebsiella) verursacht werden; es gibt Hinweise auf die wichtige Rolle pathogener Pilze, Sarcinus, Brucella und Viren. Durch diese Krankheitserreger verursachte Krankheiten sind schwerwiegender, insbesondere eine Endokarditis, die durch eine Pilzinfektion verursacht wird (tritt normalerweise aufgrund des irrationalen Einsatzes von Antibiotika auf). Bei einer Reihe von Patienten wird jedoch der wahre Erreger der Krankheit nicht nachgewiesen (die Häufigkeit negativer Blutkulturergebnisse beträgt 20–50 %). Häufig tritt eine Infektion an der Stelle einer Klappenprothese auf – das sogenannte prothetische IE, das sich hauptsächlich innerhalb von 2 Monaten nach einer Herzklappenersatzoperation entwickelt. In diesem Fall ist der Erreger der Krankheit meistens Streptokokken-Natur. So sind die Infektions- und Bakteriämiequellen bei IE sehr unterschiedlich (Operationen in der Mundhöhle, Operationen und diagnostische Eingriffe im Urogenitalbereich, chirurgische Eingriffe am Herz-Kreislauf-System (einschließlich Klappenersatz), längerer Verbleib des Katheters in einer Vene, häufige intravenöse Infusionen und endoskopische Methodenstudien, chronische Hämodialyse (arteriovenöser Shunt), intravenöse Arzneimittelverabreichung). Es gibt sogenannte primäre IE, die sich an intakten Klappen entwickelt haben, sowie IE vor dem Hintergrund angeborener und erworbener Veränderungen des Herzens und seines Klappenapparats - sekundäre Endokarditis. Diese Veränderungen ermöglichen es, Patienten in separate Risikogruppen einzuteilen: Herzfehler (angeboren und erworben), Mitralklappenprolaps, arteriovenöse Aneurysmen, Postinfarkt-Aneurysmen, Shunts, Zustand nach Operationen am Herzen und großen Gefäßen. 18. Pathogenese und Klassifikation der infektiösen Endokarditis (IE) Pathogenese. Der Mechanismus der Entwicklung von IE ist komplex und nicht gut verstanden. Bei der Entwicklung der Krankheit können 3 Stadien unterschieden werden. Stufe I (infektiös-toxisch) verläuft mit unterschiedlichem Schweregrad der Vergiftung. Es gibt ein Wachstum von Bakterien, die Zerstörung von Klappen, was zur Entwicklung von Herzkrankheiten führt; im gleichen Stadium kommt es aufgrund der hämatogenen Ausbreitung der Infektion häufig zu einer Verallgemeinerung des Prozesses - Höckerstücke oder Kolonien von Mikroorganismen können sich von der Klappe lösen, die Höcker können platzen. Stadium II - immuninflammatorisch, bei dem an den Klappen fixierte Mikroorganismen eine verlängerte Autosensibilisierung und hyperergische Schädigung der Organe und Gewebe des Körpers verursachen (Immunverallgemeinerung des Prozesses). Stadium III - dystrophisch - tritt mit dem Fortschreiten des pathologischen Prozesses auf: Die Funktionen einer Reihe von Organen sind gestört, es kommt zu Herz- und Nierenversagen, was den Krankheitsverlauf weiter verschlimmert (siehe Tabelle). Tabellenklassifizierung von IE
Außerdem wird zwischen aktivem und inaktivem (geheiltem) IE unterschieden. Es gibt auch eine chirurgische Klassifikation, in der sie unterscheiden: 1) die Läsion ist auf die Klappensegel beschränkt; 2) die Läsion erstreckt sich über die Klappe hinaus. Akute IE (schnell fortschreitend, entwickelt sich über 8-10 Wochen) ist selten, normalerweise bei Personen, die zuvor keine Herzerkrankung hatten, und manifestiert sich klinisch durch das Bild einer allgemeinen Sepsis. Subakute IE (am häufigsten) dauert 3-4 Monate, bei adäquater medikamentöser Therapie kann eine Remission eintreten. Protrahierte IE dauert viele Monate mit Exazerbations- und Remissionsperioden und ist durch milde klinische Manifestationen gekennzeichnet. Bei ungünstigem Verlauf treten schwere Komplikationen auf und die Patienten sterben an fortschreitender Herzinsuffizienz, was zu einer zunehmenden septischen Vergiftung führt. 19. Klinisches Bild und Diagnose der infektiösen Endokarditis (IE) Krankheitsbild. Die Manifestationen von IE werden als Syndrome dargestellt. 1. Syndrom entzündlicher Veränderungen und Blutvergiftung. 2. Syndrom der allgemeinen Vergiftung des Organismus. 3. Syndrom des Klappenschadens. 4. Syndrom von "Labor"-Immunstörungen. 5. Syndrom thromboembolischer Komplikationen. 6. Syndrom der Generalisierung von Läsionen. Die Diagnose einer IE basiert in erster Linie auf der Früherkennung des Erregers der Krankheit. Zu diesem Zweck werden die folgenden Labor- und Instrumentenstudien verwendet. 1. Erhalt einer positiven Blutkultur. 2. Durchführung des NBT (Nitroblautetrazolium-Test). 3. Klinischer Bluttest zum Nachweis von Akute-Phase-Indikatoren: ein Anstieg der ESR auf 50 mm / h oder mehr, Leukozytose mit einer Verschiebung der Leukozytenformel nach links oder (im Stadium II) Leukopenie und hypochrome Anämie können nachgewiesen werden. 4. Identifizierung immunologischer Veränderungen. 5. Eine Urinanalyse wird durchgeführt, um die Läsionen verschiedener Organe und Systeme zu klären, wenn eine Glomerulonephritis festgestellt wird, die sich durch Proteinurie, Zylindrurie und Hämaturie manifestiert. 6. Ein direktes diagnostisches Zeichen von IE – das Vorhandensein von Vegetation auf den Herzklappen – wird durch Echokardiographie erkannt. Aus der ganzen Vielfalt der Symptome sollten daher die Haupt- und Nebensymptome unterschieden werden. Die Hauptkriterien für die Diagnose von IE: 1) Fieber mit einer Temperatur über 38 °C mit Schüttelfrost; 2) Lukin-Flecken; 3) Osler-Knötchen; 4) Endokarditis an unveränderten Klappen (primär) oder vor dem Hintergrund rheumatischer und angeborener Herzfehler. infektiöse Myokarditis; 5) multiple arterielle Thromboembolien, Rupturen von mykotischen Aneurysmen mit Blutungen; 6) Splenomegalie; 7) positive Blutkultur; 8) ein ausgeprägter positiver Effekt durch den Einsatz von Antibiotika. Zusätzliche Kriterien für die Diagnose von IE: 1) Anstieg der Körpertemperatur auf bis zu 38 °C, Frösteln; 2) Blutungen auf der Haut; 3) schneller Gewichtsverlust; 4) asymmetrische Arthritis der kleinen Gelenke der Hände, Füße; 5) Anemisierung; 6) ESR über 40 mm/h; 7) stark positiver SRV; 8) das Vorhandensein von Rheumafaktor; 9) a-Globuline über 25 %; 10) Erhöhung des Gehalts an Immunglobulinen M, E und A. 20. Behandlung und Prävention der infektiösen Endokarditis (IE) Behandlung. Die Behandlung von IE sollte unter Berücksichtigung bakteriologischer Daten so früh und etiotrop wie möglich erfolgen. Eine Kombination aus konservativer und operativer Behandlung ist ratsam. Zur Behandlung von IE in allen Altersgruppen werden hauptsächlich Antibiotika eingesetzt, die eine bakterizide Wirkung auf Mikroorganismen haben. Das Medikament der ersten Wahl ist nach wie vor Penicillin. Die Tagesdosis - bis zu 20 IE wird intravenös und intramuskulär verabreicht. Es sollte jedoch nicht ausgeschlossen werden, dass bei älteren und senilen Patienten, wenn sie mit Penicillin und anderen Antibiotika in hohen Dosen behandelt werden, häufig eine kardiotoxische Wirkung beobachtet wird. Bei unbekannter Ätiologie beginnt die Behandlung mit hohen Dosen von Benzylpenicillin intramuskulär oder intravenös bis zu 18-000 Einheiten oder mehr, einer Kombination mit Streptomycin bis zu 000 g / m pro Tag oder Aminoglykosiden (Gentamicin, Tobramycin in einer Menge von 20-000 mg / Tag) verwendet wird. kg pro Tag). Цефалоспорины также являются базисными препаратами, применяемыми для лечения ИЭ: наиболее часто используют клафоран, цефамизин (000-1 г/сутки, внутримышечно и внутривенно), а также цепорин (4-6 г/сутки) и кефзол (до 4-10 г внутривенно usw.). Fusidin hat eine gute Anti-Staphylokokken-Wirkung, in einigen Fällen ist es bei der Resistenz von Mikroorganismen gegen andere Antibiotika wirksam (10-16 g / Tag). Die Behandlung mit Antibiotika wird über einen Zeitraum von 1,5 bis 2 Monaten verschrieben, bis die Infektion vollständig beseitigt ist. Bei verminderter Immunreaktivität des Körpers werden antibakterielle Wirkstoffe mit einer passiven Immuntherapie unter Verwendung von Immunmodulatoren (Thymalin, T-Aktivin usw.) kombiniert. Um Thrombosen vorzubeugen, beispielsweise bei einer Endokarditis, die sich vor dem Hintergrund einer angiogenen Sepsis entwickelt hat, wird eine kontrollierte Hypokoagulation mit Heparin (20-000 Einheiten intravenös oder subkutan) erzeugt. Um proteolytische Enzyme zu hemmen, wird Contrical verwendet (bis zu 25–000 Einheiten intravenös). Wenn die valvuläre IE zur Entstehung einer Herzklappenerkrankung beigetragen hat oder die Manifestationen der Erkrankung trotz massiver Antibiotikatherapie nicht verschwinden, ist eine chirurgische Behandlung ratsam. Das Hauptziel der Operation ist der Erhalt der eigenen Klappe des Patienten. Manchmal beschränken sie sich auf das Entfernen von Vegetationen, das Nähen von Klappenbrüchen usw. Wenn die Klappe unter dem Einfluss einer Infektion fast vollständig zerstört wird, wird sie durch eine künstliche Klappe (Prothese) unter Verwendung mechanischer und biologischer Prothesen ersetzt. Verhütung. Die Vorbeugung von IE besteht in der rechtzeitigen Sanierung chronischer Infektionsherde in der Mundhöhle, Mandeln, Nasopharynx, Nasennebenhöhlen, der Anwendung einer aktiven Antibiotikatherapie bei akuten Streptokokken- und Staphylokokkenerkrankungen (Tonsillitis usw.). Eine Abhärtung des Körpers wird empfohlen. 21. Ätiologie des Asthma bronchiale (BA) Eine erschöpfende Definition von Asthma existiert bis heute nicht, die vollständigste Definition dieser Krankheit wurde jedoch 1982 von G. B. Fedoseev gegeben. der wichtigste und obligatorische pathogenetische Mechanismus davon ist eine veränderte bronchiale Reaktivität aufgrund spezifischer (immunologischer) und (oder) unspezifischer, angeborener oder erworbener Mechanismen, und das wichtigste (obligatorische) klinische Zeichen ist ein Asthmaanfall und (oder) eine asthmatische Erkrankung ( asthmatischer Status) aufgrund von Krämpfen der glatten Bronchialmuskulatur, Hypersekretion, Dyskrinie und Schwellung der Bronchialschleimhaut. Ätiologie. Bei der Entstehung von Asthma spielt das Zusammenspiel mehrerer Faktoren eine wichtige Rolle. In dieser Hinsicht gibt es zwei Formen von Asthma – atopisches (von lateinisch athopia – „erbliche Veranlagung“) und infektiös-allergisches. Die erbliche Veranlagung beruht auf dem Zusammenhang bestimmter Histokompatibilitätsantigene (HCA) mit der Schwere des Asthmas, wobei eine Zunahme der Schwere der Erkrankung besonders häufig bei Trägern der Antigene B2 und B35 beobachtet wird. Interne Faktoren bei der Entwicklung der Krankheit sind biologische Defekte im Immunsystem, im endokrinen System, im vegetativen Nervensystem, in der bronchialen Sensibilität und Reaktivität, in der mukoziliären Clearance, im pulmonalen Gefäßendothel, im Rapid-Response-System (Mastzellen usw.), im Metabolismus von Arachidonsäure, usw. Zu den externen Faktoren gehören: 1) infektiöse Allergene (Viren, Bakterien, Pilze, Hefe usw.); 2) nicht infektiöse Allergene (Pollen, Staub, Industrie, Medizin, Lebensmittel; Allergene von Zecken, Insekten und Tieren); 3) mechanische und chemische Reizstoffe (Metall-, Holz-, Silikat-, Baumwollstaub; Dämpfe von Säuren, Laugen; Dämpfe usw.); 4) meteorologische und physikalisch-chemische Faktoren (Änderungen der Lufttemperatur und -feuchtigkeit, Schwankungen des Luftdrucks, des Erdmagnetfelds, körperliche Anstrengung usw.); 5) stressige, neuropsychische Wirkungen und körperliche Aktivität. Infektionserreger können nicht nur allergen wirken, sondern auch die Empfindlichkeitsschwelle des Körpers gegenüber nicht infektiösen (atopischen) Allergenen senken, die Durchlässigkeit der Atemwegsschleimhaut für sie erhöhen; eine Veränderung der Reaktivität von Zielzellen (Mastzellen, Basophilen, Monozyten etc.) und Effektorsystemen zu bilden. 22. Pathogenese von Asthma bronchiale (BA) Pathogenese. Eine veränderte bronchiale Reaktivität ist das zentrale Glied in der Pathogenese der Krankheit und kann primär und sekundär sein. Im ersten Fall ist die Veränderung der Reaktivität angeboren und erworben. Sekundäre Veränderungen der bronchialen Reaktivität sind eine Manifestation von Veränderungen in der Reaktivität des Immunsystems, des endokrinen und des Nervensystems des Körpers. Wenn wir also über die Pathogenese von AD sprechen, können wir zwei Gruppen von Mechanismen unterscheiden: immunologische und nicht-immunologische. Typ I (atopisch, reaginisch oder anaphylaktisch). Als Reaktion auf die Aufnahme von Exoallergen-Antigenen (Pollen, tierische und pflanzliche Proteine, Bakterien und Medikamente) kommt es zu einer erhöhten Produktion (Reagine), die auf Mastzellen (primäre Effektorzellen) fixiert und angereichert werden. Dies ist das immunologische Stadium von AD. Anschließend entwickelt sich das pathochemische Stadium des Prozesses - Degranulation von Mastzellen mit Freisetzung von vasoaktiven, bronchospastischen und chemotaktischen Substanzen (Histamin, Serotonin, verschiedene chemotaktische Faktoren usw.). Unter dem Einfluss biologisch aktiver Substanzen beginnt das pathophysiologische Stadium der Pathogenese: Die Durchlässigkeit des Mikrozirkulationsbetts nimmt zu, was zur Entwicklung von Ödemen, serösen Entzündungen und Bronchospasmen führt. Die Typ-III-Reaktion (Immunkomplex-Typ oder Arthus-Phänomen) entwickelt sich unter dem Einfluss von Exoallergenen und Endoallergenen. Die Reaktion erfolgt in der Zone des überschüssigen Antigens unter Beteiligung präzipitierender Antikörper, die zu den Immunglobulinen der Klassen O und M gehören. Die schädigende Wirkung des gebildeten Antigen-Antikörper-Komplexes wird durch Komplementaktivierung, die Freisetzung lysosomaler Enzyme, realisiert. Es kommt zu einer Schädigung der Basalmembranen, einem Krampf der glatten Muskulatur der Bronchien, einer Vasodilatation und einer Zunahme der Durchlässigkeit der Mikrogefäße. Typ IV (zelluläre Hypersensitivität vom verzögerten Typ) ist dadurch gekennzeichnet, dass sensibilisierte Lymphozyten schädigend wirken. In diesem Fall sind die Mediatoren der allergischen Reaktion Lymphokine (wirken auf Makrophagen, Epithelzellen), lysosomale Enzyme und ein aktiviertes Kininsystem. Unter dem Einfluss dieser Substanzen entwickeln sich Ödeme, Schleimhautschwellungen, Bronchospasmen, Hyperproduktion von viskosen Bronchialsekreten. Nicht-immunologische Mechanismen sind die primäre Veränderung der bronchialen Reaktivität als Ergebnis angeborener und erworbener biologischer Defekte. Nicht-immunologische Mechanismen wirken auf primäre oder sekundäre Effektorzellen oder auf die Rezeptoren der glatten Muskulatur der Bronchien, Blutgefäße, Zellen der Bronchialdrüsen. Dadurch verändert sich die Reaktionsfähigkeit von Zielzellen und vor allem Mastzellen, was mit einer übermäßigen Produktion biologisch aktiver Substanzen (Histamin, Leukotriene etc.) einhergeht. В последнее время говорят об особой роли в патогенезе нарушений бронхиальной проходимости глюкокортикоидной недостаточности и дизовариальных расстройств. Недостаточность глюкокортикостероидов приводит к развитию гиперреактивности тучных клеток, снижению синтеза катехоламинов, активации простагландинов F2a, а также нарушению иммунокомпетентной системы. 23. Klassifikation Asthma bronchiale (BA) Einstufung. Das Vorherrschen des einen oder anderen Mechanismus in der Pathogenese von AD ermöglicht es, seine verschiedenen pathogenetischen Merkmale zu unterscheiden. Derzeit wird die von G. B. Fedoseev (1982) vorgeschlagene Klassifikation verwendet. Stadien der AD-Entwicklung. I - Präasthma (Zustände, die die Entwicklung bedrohen: akute und chronische Bronchitis, akute und chronische Lungenentzündung mit Elementen von Bronchospasmus in Kombination mit vasomotorischer Rhinitis, Urtikaria). II – klinisch gebildeter BA (wird als solcher nach dem ersten Anfall oder dem unmittelbaren Einsetzen des Status asthmaticus betrachtet). BA-Formulare: 1) immunologisch; 2) nicht-immunologisch. Pathogenetische Mechanismen (klinische und pathogenetische Varianten) von AD: 1) atopisch; 2) infektionsabhängig; 3) Autoimmun; 4) deshormonell; 5) neuropsychisches Ungleichgewicht; 6) adrenerges Ungleichgewicht; 7) cholinerges Ungleichgewicht; 8) primäre veränderte bronchiale Reaktivität. Schweregrad von BA: 1) milder Verlauf (Exazerbationen sind selten, 2-3 mal im Jahr, kurzfristige Asthmaanfälle werden durch die Einnahme verschiedener Bronchodilatatoren im Inneren gestoppt); 2) moderat (häufigere Exazerbationen 3-4 Mal im Jahr, Asthmaanfälle sind schwerer und werden durch Injektionen von Medikamenten gestoppt); 3) schwerer Verlauf (gekennzeichnet durch häufige und anhaltende Exazerbationen, schwere Anfälle, die oft in einen asthmatischen Zustand übergehen). Phasen des Asthmaverlaufs: 1) Exazerbation (das Vorhandensein von wiederkehrenden Asthmaanfällen oder asthmatischen Zuständen); 2) abklingende Exazerbation (Schübe werden seltener und milder, körperliche und funktionelle Krankheitszeichen sind weniger ausgeprägt als in der Exazerbationsphase); 3) Remission (typische Manifestationen von BA verschwinden: Asthmaanfälle treten nicht auf; bronchiale Durchgängigkeit wird vollständig oder teilweise wiederhergestellt). Komplikationen: 1) pulmonal: Emphysem, Lungeninsuffizienz, Atelektase, Pneumothorax, Status asthmaticus usw.; 2) extrapulmonal: Cor pulmonale (kompensiert und dekompensiert mit der Entwicklung einer Rechtsherzinsuffizienz), Myokarddystrophie usw. 24. Differentialdiagnose Asthma bronchiale (BA) Differenzialdiagnose. BA wird von Herzasthma unterschieden (siehe Tabelle 1). Tabelle 1 Differentialdiagnose von AD
25. Behandlung und Vorbeugung von Asthma bronchiale (BA) Behandlung. Bei der Behandlung von Asthma wird ein schrittweises Vorgehen empfohlen (Stufe 1 – der geringste Schweregrad des Asthmas, Stufe 4 – der stärkste). Schritt 1: Ein milder intermittierender Verlauf, bei dem Asthmasymptome bei Exposition gegenüber einem Auslöser (z. B. Pollen oder Tierhaare) oder aufgrund von körperlicher Anstrengung auftreten. Die Behandlung besteht aus prophylaktischen Medikamenten, falls erforderlich (Inhalationsmedikamente werden verschrieben - Agonisten, Cromoglycat, Nedocromil oder Anticholinergika). Wenn sich Asthma mit häufigeren Symptomen und einem erhöhten Bedarf an Bronchodilatatoren manifestiert, muss zur nächsten Stufe übergegangen werden. Stufe 2. Leicht anhaltender Verlauf. Die Primärtherapie umfasst entzündungshemmende Medikamente, inhalative Kortikosteroide, Natriumcromoglycat oder Nedocromil-Natrium. Bei schwereren und länger andauernden Exazerbationen wird eine kurze Behandlung mit oralen Kortikosteroiden durchgeführt. Stadium 3 ist durch einen moderaten Schweregrad von BA gekennzeichnet. Solche Patienten benötigen eine tägliche Einnahme von prophylaktischen entzündungshemmenden Arzneimitteln. Die Dosis von inhalativen Kortikosteroiden beträgt 800-2000 mcg in Kombination mit langwirksamen Bronchodilatatoren. Stadium 4. Schweres Asthma, wenn es nicht vollständig unter Kontrolle ist. In diesem Fall ist das Ziel der Behandlung, bestmögliche Ergebnisse zu erzielen. Die Primärbehandlung beinhaltet die Ernennung von inhalativen Kortikosteroiden in hohen Dosen. Eine schwerere Exazerbation kann eine Behandlung mit oralen Kortikosteroiden erfordern, die in minimalen Dosen oder jeden zweiten Tag verschrieben werden. Um die Entwicklung von Nebenwirkungen zu verhindern, werden hohe Dosen von inhalativen Kortikosteroiden über einen Abstandshalter verabreicht. Schritt 5 beinhaltet die Reduzierung unterstützender Medikamente. Dies ist möglich, wenn das Asthma mindestens 3 Monate unter Kontrolle bleibt, was dazu beiträgt, das Risiko von Nebenwirkungen zu verringern und die Anfälligkeit des Patienten für die geplante Behandlung zu erhöhen. "Reduktion" der Behandlung wird unter ständiger Kontrolle von Symptomen, klinischen Manifestationen und Indikatoren der Atemfunktionen durchgeführt, indem die letzte Dosis oder zusätzliche Medikamente schrittweise reduziert (aufgehoben) werden. Verhütung. Die Primärprävention von Asthma umfasst die Behandlung von Patienten in einem Prä-Asthma-Zustand, die Erkennung von biologischen Defekten bei praktisch gesunden Personen mit einer belasteten Vererbung, die eine Gefahr für den Ausbruch von Asthma darstellen, die Eliminierung potenziell gefährlicher Allergene, Reizstoffe und anderer Faktoren aus dem Umfeld der Patienten, die zur Entstehung der Krankheit führen können. Bei der Behandlung von Patienten in einem Zustand von Preasthma ist es notwendig, die Infektionsherde zu desinfizieren, allergische Rhinosinusopathie zu behandeln, verschiedene Methoden der nicht-medikamentösen Behandlung anzuwenden, einschließlich Akupunktur und Psychotherapie, Bewegungstherapie, Barotherapie, Spa-Behandlung. Es ist die Durchführung der spezifischen und nicht spezifischen Hyposensibilisierung vorgeführt. 26. Ätiologie und Pathogenese der chronischen Bronchitis (CB) Die chronisch obstruktive Bronchitis ist eine diffuse nicht allergische entzündliche Läsion des Bronchialbaums, verursacht durch anhaltende Reizwirkung auf die Bronchien verschiedener Wirkstoffe, die einen progressiven Verlauf hat und durch obstruktive Lungenventilation, Schleimbildung und die Drainagefunktion der Bronchien gekennzeichnet ist Baum, der sich durch Husten, Auswurf und Atemnot äußert. Chronische Bronchitis wird in primäre und sekundäre unterteilt. Primäre chronische Bronchitis ist eine eigenständige Erkrankung, die nicht mit anderen bronchopulmonalen Prozessen oder Schäden an anderen Organen und Systemen verbunden ist, bei denen eine diffuse Läsion des Bronchialbaums vorliegt. Sekundäres HB entwickelt sich vor dem Hintergrund anderer Erkrankungen - sowohl pulmonal als auch extrapulmonal. Ätiologie. Bei der Entstehung von CB spielen zB exogene Faktoren eine Rolle. Das obstruktive Syndrom entwickelt sich aufgrund einer Kombination mehrerer Faktoren: 1) Krämpfe der glatten Muskulatur der Bronchien als Folge irritierender Wirkungen exogener Faktoren und entzündlicher Veränderungen der Schleimhaut; 2) Hypersekretion von Schleim, Veränderungen seiner rheologischen Eigenschaften, die zu einer Störung des mukoziliären Transports und einer Verstopfung der Bronchien mit einem viskosen Geheimnis führen; 3) Epithelmetaplasie von zylindrischem bis stratifiziertem Plattenepithel und dessen Hyperplasie; 4) Verstöße gegen die Herstellung von Tensiden; 5) entzündliches Ödem und Schleimhautinfiltration; 6) Kollaps der kleinen Bronchien und Verödung der Bronchiolen; 7) allergische Veränderungen der Schleimhaut. Verschiedene Verhältnisse von Veränderungen in der Schleimhaut verursachen die Bildung einer bestimmten klinischen Form: 1) bei katarrhalischer nicht obstruktiver Bronchitis überwiegen oberflächliche Veränderungen der strukturellen und funktionellen Eigenschaften der Schleimhaut; 2) bei mukopurulenter (eitriger) Bronchitis überwiegen die Prozesse der infektiösen Entzündung. Es ist aber auch möglich, dass eine lang anhaltende katarrhalische Bronchitis durch Hinzufügung einer Infektion schleimig-eitrig werden kann usw. Bei der nicht-obstruktiven Variante aller klinischen Formen der chronischen Bronchitis sind Ventilationsstörungen leicht ausgeprägt; 3) obstruktive Störungen treten zunächst nur vor dem Hintergrund einer Verschlimmerung der Erkrankung auf und werden durch entzündliche Veränderungen der Bronchien, Hyper- und Dyskrinie, Bronchospasmus (reversible Komponenten der Obstruktion) verursacht, bleiben dann aber konstant bestehen, während das obstruktive Syndrom zunimmt langsam. 27. Klinisches Bild der chronischen Bronchitis (CB) Krankheitsbild. Die Hauptsymptome von HB sind Husten, Auswurf, Kurzatmigkeit. Bei einer Verschlimmerung der Krankheit oder aufgrund von Hypoxie mit der Entwicklung einer Lungeninsuffizienz und anderen Komplikationen werden allgemeine Symptome (Schwitzen, Schwäche, Fieber, Müdigkeit usw.) aufgedeckt. Husten ist die typischste Manifestation der Krankheit. Je nach Art und Konsistenz des Sputums kann man von einer Variante des Krankheitsverlaufs ausgehen. Bei einer nicht obstruktiven Variante der katarrhalischen Bronchitis wird der Husten von einer kleinen Menge schleimigem wässrigem Auswurf begleitet (häufiger morgens, nach körperlicher Anstrengung oder durch vermehrte Atmung). Zu Beginn der Krankheit stört Husten den Patienten nicht; das Auftreten eines paroxysmalen Hustens weist auf die Entwicklung einer Bronchialobstruktion hin. Der Husten nimmt einen bellenden Schatten an und ist paroxysmaler Natur mit einem ausgeprägten Ausatmungskollaps der Luftröhre und großen Bronchien. Bei eitriger und schleimig-eitriger Bronchitis sind die Patienten eher besorgt über das Abhusten von Sputum. Im Falle einer Verschlimmerung der Krankheit nimmt der Auswurf einen eitrigen Charakter an, seine Menge nimmt zu, manchmal wird der Auswurf mit Schwierigkeiten ausgeschieden (aufgrund einer Bronchialobstruktion während der Verschlimmerung). Bei der obstruktiven Variante der Bronchitis ist der Husten unproduktiv und hackend, begleitet von Atemnot, mit etwas Auswurf. Kurzatmigkeit tritt bei allen Patienten mit chronischer Bronchitis zu unterschiedlichen Zeiten auf. Das Auftreten von Atemnot bei „Langzeithusten“-Patienten mit anfänglich erheblicher körperlicher Anstrengung deutet auf eine zusätzlich bronchiale Obstruktion hin. Mit fortschreitender Erkrankung wird die Atemnot ausgeprägter und konstanter, d.h. es entwickelt sich eine respiratorische (pulmonale) Insuffizienz. Bei der nicht-obstruktiven Variante schreitet CB langsam voran, Atemnot tritt meist 20-30 Jahre nach Ausbruch der Erkrankung auf. Solche Patienten beheben fast nie den Ausbruch der Krankheit, sondern weisen nur auf das Auftreten von Komplikationen oder häufigen Exazerbationen hin. Es gibt eine Vorgeschichte von Überempfindlichkeit gegen Kälte, und die meisten Patienten berichten über langjähriges Rauchen. Bei einer Reihe von Patienten ist die Krankheit mit Berufsrisiken bei der Arbeit verbunden. Bei der Analyse einer Hustenanamnese muss sichergestellt werden, dass der Patient keine andere Pathologie des Bronchopulmonalapparats (Tuberkulose, Tumore, Bronchiektasen, Pneumokoniose, systemische Erkrankungen des Bindegewebes usw.) hat, die von denselben Symptomen begleitet werden. Manchmal weist eine Anamnese auf eine Hämoptyse aufgrund einer leichten Anfälligkeit der Bronchialschleimhaut hin. Rezidivierende Hämoptysen weisen auf eine hämorrhagische Form der Bronchitis hin. Darüber hinaus kann Hämoptyse bei chronischer, langfristiger Bronchitis das erste Symptom von Lungenkrebs oder Bronchiektasen sein. 28. Diagnose einer chronischen Bronchitis (CB) Diagnose. Die Auskultation zeigt hartes Atmen (mit der Entwicklung eines Emphysems kann es geschwächt werden) und trockene Rasseln diffuser Natur, deren Klangfarbe vom Kaliber der betroffenen Bronchien abhängt (keuchendes Keuchen, das beim Ausatmen gut zu hören ist, ist charakteristisch für kleine Läsionen Bronchien). Mit einer Verschlimmerung der obstruktiven Bronchitis nimmt die Atemnot zu, die Phänomene des Atemversagens nehmen zu. In fortgeschrittenen Fällen von chronischer Bronchitis und mit zusätzlichen Komplikationen treten Anzeichen eines Lungenemphysems, respiratorischer und kardialer (rechtsventrikulärer) Insuffizienz - dekompensiertes Lungenherz auf: Akrozyanose, Pastosität oder Schwellung der Beine und Füße, Veränderungen der Nägel in die Form von Uhrgläsern und die Endphalangen der Hände und Füße - in Form von Trommelstöcken, Schwellung der Halsvenen, Pulsieren in der Magengegend aufgrund des rechten Ventrikels, Akzent des II-Tons im II-Interkostal Raum links vom Brustbein, Lebervergrößerung. Labor- und instrumentelle Indikatoren haben je nach Prozessstufe unterschiedliche Aussagekraft. Bei allen Patienten mit chronischer Bronchitis wird eine Röntgenuntersuchung der Brustorgane durchgeführt, in der Regel treten jedoch auf Röntgenaufnahmen keine Veränderungen in der Lunge auf. Aufgrund der Entwicklung einer Pneumosklerose kann es zu einer Maschenverformung des Lungenmusters kommen. Die Röntgenuntersuchung spielt eine wichtige Rolle bei der Diagnose von Komplikationen (akute Lungenentzündung, Bronchiektasen) und bei der Differentialdiagnose bei Erkrankungen mit ähnlichen Symptomen. Bronchographie wird nur verwendet, um Bronchiektasen zu diagnostizieren. Die Bronchoskopie ist von großer Bedeutung für die Diagnostik der chronischen Bronchitis und deren Abgrenzung zu Erkrankungen mit ähnlichem Krankheitsbild. Es bestätigt das Vorhandensein eines entzündlichen Prozesses; klärt die Art der Entzündung; zeigt Funktionsstörungen des Tracheobronchialbaums; hilft bei der Identifizierung organischer Läsionen des Bronchialbaums. Die Untersuchung der Funktion der äußeren Atmung wird durchgeführt, um restriktive und obstruktive Störungen der Lungenventilation zu identifizieren. Gemäß dem Spirogramm werden der Tiffno-Index und der Luftgeschwindigkeitsindikator - PSDV berechnet. Auch die gemeinsame Beurteilung von Bronchialwiderstand und Lungenvolumen hilft, den Grad der Obstruktion zu bestimmen. Eine Radiopulmonographie mit dem radioaktiven Isotop 133Xe wird durchgeführt, um eine ungleichmäßige Belüftung im Zusammenhang mit einer Obstruktion der kleinen Bronchien zu erkennen. Eine Elektrokardiographie ist notwendig, um eine Hypertrophie des rechten Ventrikels und des rechten Vorhofs zu erkennen, die sich bei pulmonaler Hypertonie entwickelt. Ein klinischer Bluttest zeigt eine sekundäre Erythrozytose, die aus einer chronischen Hypoxie mit der Entwicklung einer schweren Lungeninsuffizienz resultiert. "Akutphase" -Indikatoren werden mäßig ausgedrückt. Die mikrobiologische Untersuchung von Sputum und Bronchialinhalt ist wichtig, um die Ätiologie von Exazerbationen einer chronischen Bronchitis und die Wahl einer antimikrobiellen Therapie zu identifizieren. 29. Differentialdiagnose der chronischen Bronchitis (CB) Tabelle Differenzialdiagnostische Kriterien für CB
30. Behandlung der chronischen Bronchitis (CB) Behandlung. Es umfasst eine Reihe von Maßnahmen, die sich während der Zeit der Exazerbation und Remission der Krankheit unterscheiden. Bei der Exazerbation einer chronischen Bronchitis werden zwei Behandlungsrichtungen unterschieden: ätiotrop und pathogenetisch. Die etiotrope Behandlung zielt darauf ab, den Entzündungsprozess in den Bronchien zu beseitigen: Indiziert ist eine Therapie mit Antibiotika, Sulfanilamid-Medikamenten, Antiseptika, Phytonziden usw. Die Behandlung beginnt mit Antibiotika der Penicillin-Reihe (Penicillin, Ampicillin) oder einer Gruppe von Cephalosporinen (Cefamesin , tseporin), und in Ermangelung einer Wirkung werden Antibiotika der Gruppe Reserve (Gentamicin usw.) verwendet. Der am meisten bevorzugte Verabreichungsweg ist intratracheal (Aerosol oder Füllung mit einer Larynxspritze durch ein Bronchoskop). Die pathogenetische Behandlung zielt darauf ab, die Lungenventilation zu verbessern; Wiederherstellung der bronchialen Durchgängigkeit; Kontrolle der pulmonalen Hypertonie und des rechtsventrikulären Versagens. Die Wiederherstellung der Lungenventilation wird neben der Beseitigung des Entzündungsprozesses in den Bronchien durch Sauerstofftherapie und Bewegungstherapie erleichtert. Die Hauptsache bei der Behandlung von chronischer Bronchitis - die Wiederherstellung der Durchgängigkeit der Bronchien - wird durch die Verbesserung ihrer Drainage und die Beseitigung von Bronchospasmen erreicht. Zur Verbesserung der Bronchialdrainage werden Expektorantien (heißes alkalisches Getränk, Kräutersud, Mukaltin usw.), Mukolytika (Acetylcystein, Bromhexin; mit eitriger viskoser Sekretion - Aerosole proteolytischer Enzyme - Chymopsin, Trypsin) verschrieben; therapeutische Bronchoskopie verwendet wird. Zur Beseitigung von Bronchospasmus wird Eufillin (intravenös, in Zäpfchen, Tabletten), Ephedrin, Atropin verwendet; Einzeltermine in einem Aerosol von Sympathomimetika sind möglich: Fenoterol, Orciprenalinsulfat (Asthmopenta) und ein neues Inlandsmedikament "Soventol", Anticholinergika: Atrovent, Troventol. Wirksame Präparate mit verlängertem Aminophyllin (Teopec, Teodur, Theobelong usw.) - 2 mal täglich. In Ermangelung der Wirkung einer solchen Therapie werden kleine Dosen von Kortikosteroiden oral (10-15 mg Prednisolon pro Tag) oder intratracheal (Hydrocortisonsuspension - 50 mg) verabreicht. Als zusätzliche Therapie ernennen Sie: 1) Antitussiva: bei unproduktivem Husten - Libexin, Tusuprex, Bromhexin, bei Hackhusten - Codein, Dionin, Stoptussin; 2) Medikamente, die die Widerstandskraft des Körpers erhöhen: Vitamine A, C, Gruppe B, biogene Stimulanzien. Derzeit werden bei der Behandlung von chronischer Bronchitis zunehmend immunkorrigierende Medikamente eingesetzt: T-Aktivin oder Thymalin (100 mg subkutan für 3 Tage); innen - Catergen, Natriumnucleinat oder Pentoxyl (innerhalb von 2 Wochen), Levamisol (Decaris). Physiotherapeutische Behandlung: Verschreiben Sie Diathermie, Calciumchlorid-Elektrophorese, Quarz im Brustbereich, Brustmassage und Atemübungen. 31. Lungenentzündung. Ätiologie, Pathogenese, Klassifikation Pneumonie ist eine akute infektiöse und entzündliche Erkrankung fokaler Natur, bei der die Atemwege und das interstitielle Bindegewebe der Lunge am pathologischen Prozess beteiligt sind. Klassifizierung von E. V. Gembitsky (1983). Nach Ätiologie: 1) bakteriell (zeigt den Erreger an); 2) viral (zeigt den Erreger an); 3) Kornit; 4) Rickettsien; 5) Mykoplasmen; 6) Pilz; 7) gemischt; 8) infektiös-allergisch; 9) unbekannte Ätiologie. Nach Pathogenese: 1) primär; 2) sekundär. Klinische und morphologische Merkmale: 1) Parenchym: kruppig; fokal; 2) Zwischenraum. Nach Lokalisation und Ausdehnung: einseitig; zweiseitig. Nach Schweregrad: extrem schwer; schwer; mäßig; mild und abortiv. Stromabwärts: scharf; langwierig (radiologische und klinische Auflösung der Lungenentzündung). Ätiologie. Die meisten Lungenentzündungen sind infektiösen Ursprungs. Allergische Lungenentzündungen, die durch die Einwirkung physikalischer oder chemischer Faktoren verursacht werden, sind selten. Bakterielle Lungenentzündungen werden häufiger bei Menschen mittleren Alters und älteren Menschen diagnostiziert; Viruspneumonie - bei jungen Menschen. In der Ätiologie der primären bakteriellen Pneumonie gehört Pneumokokken die führende Rolle. Während einer Influenza-Epidemie nimmt die Rolle viral-bakterieller Assoziationen (normalerweise Staphylokokken) sowie opportunistischer Mikroorganismen zu. Bei der sekundären Pneumonie spielen gramnegative Bakterien (Klebsiella pneumoniae und Influenza-Bazillus) die führende ätiologische Rolle; Beim Auftreten einer Aspirationspneumonie ist die Bedeutung einer anaeroben Infektion groß. Pathogenese. Der Infektionserreger gelangt von außen durch die Bronchien in die Atemwege der Lunge: Inhalation und Aspiration (aus dem Nasopharynx oder Oropharynx). Auf hämatogenem Weg gelangt der Erreger vor allem bei sekundärer Pneumonie oder bei der thrombotischen Genese einer Pneumonie in die Lunge. Die lymphogene Ausbreitung der Infektion mit dem Beginn einer Lungenentzündung wird nur bei Verletzungen der Brust beobachtet. Auch allergischen und autoallergischen Reaktionen kommt in der Pathogenese der Pneumonie eine bedeutende Bedeutung zu. 32. Diagnose einer Lungenentzündung Am bedeutsamsten für die Diagnose ist das Vorhandensein eines Syndroms entzündlicher Veränderungen im Lungengewebe. Dieses Syndrom besteht aus den folgenden Symptomen: 1) Atemverzögerung der betroffenen Brustseite; 2) mehr oder weniger starke Verkürzung des Perkussionsklangs im Bereich der Projektion der Läsion; 3) verstärktes Zittern der Stimme und Bronchophonie im selben Bereich; 4) Veränderung in der Art der Atmung (hart, bronchial, geschwächt usw.); 5) das Auftreten pathologischer Atemgeräusche (feuchtes, stimmhaftes, fein sprudelndes Rasseln und Crepitation). Die Art der Atmung kann sich auf unterschiedliche Weise verändern. Im Anfangsstadium einer croupösen Pneumonie kann die Atmung mit verlängerter Ausatmung geschwächt sein; in der Hepatisierungsphase ist zusammen mit einer Zunahme der Dumpfheit des Perkussionsklangs eine Bronchialatmung zu hören; Mit der Auflösung des pneumonischen Fokus mit einer Abnahme der Dumpfheit der Perkussion wird die Atmung schwer. Symptome helfen, eine ätiologische Diagnose zu stellen: 1) der Nachweis eines kleinfleckigen Hautausschlags wie bei Röteln in Kombination mit einer Lymphadenopathie ist charakteristisch für eine Adenovirusinfektion; 2) lokale Vergrößerung der Lymphknoten weist auf perifokale Pneumonie hin; 3) Pilzpneumonie kombiniert mit Läsionen der Schleimhäute, Haut und Nägel; 4) hepatolienales Syndrom und leichter Ikterus werden bei kornitischen und Curickettsial-Pneumonien gefunden; 5) Bei einer typischen croupösen Lungenentzündung ist das Aussehen des Patienten charakteristisch: ein blasses Gesicht mit fiebriger Rötung an der Seite der Läsion, herpetische Eruptionen, Schwellung der Nasenflügel beim Atmen. Die wichtigste Methode, um das Vorliegen einer Lungenentzündung und den Grad der Beteiligung des Lungengewebes am Prozess abzuklären, ist die großformatige Fluorographie und Röntgenuntersuchung der Brustorgane. Die Bronchographie zeigt Karieshöhlen im Lungengewebe sowie das Vorhandensein von Bronchiektasen, um die herum bei Exazerbation infiltrative Veränderungen (perifokale Pneumonie) möglich sind. Bakteriologische Untersuchung von Sputum (oder Bronchialspülungen) vor der Ernennung von Antibiotika hilft, den Erreger zu erkennen und seine Empfindlichkeit gegenüber Antibiotika zu bestimmen. Die Schwere des Entzündungsprozesses wird anhand der Schwere der Blutparameter in der akuten Phase und ihrer Dynamik beurteilt (Leukozytose mit Verschiebung der Leukozytenformel, Erhöhung der ESR, erhöhter Gehalt an a2-Globulinen, Fibrinogen, Auftreten von SRV, eine Erhöhung des Gehalts an Sialinsäuren). Bei längerem Verlauf einer Lungenentzündung und der Entwicklung von Komplikationen wird die immunologische Reaktivität des Körpers untersucht. 33. Behandlung von Lungenentzündung Behandlung. Unmittelbar nach der Diagnosestellung muss mit der etiotropen Therapie der Lungenentzündung begonnen werden. Von großer Bedeutung sind empirische Vorstellungen über einen möglichen Erreger, da die bakteriologische Untersuchung von Sputum schon seit geraumer Zeit durchgeführt wird und bei den meisten Patienten selbst bei einem modernen Ansatz dieser Studie unsichere und manchmal fehlerhafte Ergebnisse liefert. Penicilline haben derzeit ihre Bedeutung als Mittel der Wahl bei der Behandlung von Lungenentzündungen verloren. Im Zusammenhang mit dem Vorstehenden wird bei der Behandlung von Pneumonie Makroliden viel Aufmerksamkeit geschenkt, die sich nicht nur gegen Pneumococcus, sondern auch gegen Mycoplasma pneumoniae, Chlamydia pneumoniae als wirksam erwiesen haben. Dosierung von Antibiotika zur Behandlung von Lungenentzündungen. 1. Penicilline: Benzylpenicillin (500–000 IE intravenös alle 1–000 Stunden oder 000–6 IE alle 8 Stunden intramuskulär), Ampicillin (500–000–1 g intramuskulär alle 000–000 Stunden oder 4 g alle 0,5 Stunden intravenös), Amoxicillin (1,0-2,0 g alle 6 Stunden oral oder 8-0,5 g alle 6-0,5 Stunden intramuskulär, intravenös), Oxacillin (1,0 g alle 8-0,5 Stunden oral, intramuskulär, intravenös). 2. Cephalosporine: I. Generation - Cephalothin (Keflin) (0,5-2,0 g alle 4-6 Stunden intramuskulär, intravenös), Cefazolin (Kefzol) (0,5-2,0 g, alle 8 Stunden intramuskulär, intravenös ), II. Generation - Cefuroxim (Zinacef , Ketocef) (0,75-1,5 g alle 6-8 Stunden intramuskulär, intravenös), III. Generation - Cefotaxim (Claforan) (1,0-2,0 g, maximal bis zu 12 g / Tag alle 12 Stunden intramuskulär, intravenös), Ceftriaxon (Longacef, Rocefin) (1,0-2,0-4,0 g alle 24 Stunden intramuskulär, intravenös). 3. Aminoglykoside: Genetamycin (80 mg alle 12 Stunden IM, IV), Amikacin (10-15 mg/kg alle 12 Stunden IM, IV), Tobramycin (Brulamycin) (3-5 mg/kg alle 8 Stunden IM, IV) . 4. Makrolide: Erythromycin (0,5 g alle 6–8 Stunden oral oder 0,5–1,0 g alle 6–8 Stunden intravenös), Rovamycin (3,0 Millionen IE alle 8–12 Stunden oral oder 1,5–3,0 Millionen IE alle 8–12 Stunden intravenös). 5. Fluorchinolone: Pefloxacin (Leflacin) (400 mg alle 12 Stunden oral, IV), Ciprofloxacin (Cyprobay) (500 mg alle 12 Stunden oral oder 200–400 mg alle 12 Stunden intravenös), Ofloxacin (Zanocin, Tarivid) (200 mg alle 12 Stunden oral). 6. Tetracycline: Doxycyclin (Vibramycin) (200 mg am Tag 1, an den Folgetagen – 100 mg alle 24 Stunden oral), Minocyclin (Minocin) (200 mg am Tag 1, an den Folgetagen – 100 mg alle 12 Stunden oral), Aztreonam (Azactam) (1,0–2,0 g alle 8–12 Stunden), Imipenem/Cilstatin (Thienam) (500 mg alle 6–8 Stunden intramuskulär). 34. Ätiologie, Pathogenese, Krankheitsbild der akuten Ösophagitis Akute Ösophagitis ist eine entzündliche Läsion der Schleimhaut der Speiseröhre, die mehrere Tage bis 2-3 Monate dauert. Ätiologie und Pathogenese. Ätiologische Faktoren: Infektionskrankheiten, Verletzungen, Verbrennungen, Vergiftungen, allergische Reaktionen, Ernährungsfehler. Von den Infektionserregern sind Diphtherie, Scharlach, Typhus und Typhus, Influenza, Parainfluenza, Adenovirus-Infektion, Mumps die charakteristischsten für akute Ösophagitis. Physikalische und chemische Schädigungsfaktoren werden durch ionisierende Strahlung, Verätzungen, heiße und sehr kalte Speisen sowie Gewürze repräsentiert. Krankheitsbild. Die katarrhalische Ösophagitis ist die häufigste Form der akuten Ösophagitis. Es tritt vor dem Hintergrund von Ernährungsfehlern auf: Beim Essen von würzigen, kalten, warmen Gerichten, bei leichten Verletzungen, Alkoholverbrennungen. Es äußert sich klinisch durch Brennen und Schmerzen hinter dem Brustbein, was die Patienten dazu zwingt, mehrere Tage lang Nahrung zu verweigern. Endoskopisch festgestellte Ösophagitis I-II Grad, Röntgen - Hyperkinesie der Speiseröhre. Erosive Ösophagitis tritt bei Infektionskrankheiten und Allergien auf. Die klinischen Symptome ähneln denen einer katarrhalischen Ösophagitis. Die hämorrhagische Ösophagitis ist eine seltene klinische Form der erosiven Ösophagitis. Die Ätiologie ist die gleiche wie bei der erosiven Ösophagitis. Klinisch typisch sind ein intensives Schmerzsyndrom und Hämatemesis. Die Klinik wird von Dysphagie und starken Schmerzen dominiert, die sich nach dem Essen, Übelkeit und Erbrechen verschlimmern. Beim Erbrechen werden Fibrinfilme freigesetzt, es kann zu Bluthusten kommen. Membranöse (exfoliative) Ösophagitis ist von der Ätiologie her chemisch (Verbrennungen der Speiseröhre), ansteckend. In der Klinik der schweren membranösen Ösophagitis überwiegen Intoxikation, Dysphagie und Schmerzsyndrom. Die nekrotisierende Ösophagitis ist eine seltene Form der akuten Entzündung der Speiseröhre. Seine Entwicklung wird durch eine verringerte Immunität bei so schweren Krankheiten wie Sepsis, Typhus, Candidiasis und Nierenversagen im Endstadium erleichtert. Die Klinik ist gekennzeichnet durch schmerzhafte Dysphagie, Erbrechen, allgemeine Schwäche, Blutungen, häufige Entwicklung von Mediastinitis, Pleuritis, Lungenentzündung. Septische Ösophagitis ist eine seltene lokale oder diffuse Entzündung der Wände der Speiseröhre mit Streptokokken-Ätiologie oder tritt auf, wenn die Schleimhaut durch einen Fremdkörper beschädigt wird, mit Verbrennungen, Ulzerationen und kann von benachbarten Organen ausgehen. Manchmal tritt eine akute phlegmonöse Ösophagitis als Komplikation einer akuten Ösophagitis auf, die zu einer eitrigen Verschmelzung der Wände der Speiseröhre führt. Das Krankheitsbild ist gekennzeichnet durch starke Vergiftung, hohes Fieber, Schmerzen hinter dem Brustbein und im Nacken, Erbrechen. Bei der Untersuchung ist der Hals geschwollen, die Beweglichkeit in diesem Teil der Wirbelsäule ist eingeschränkt. Die Position des Kopfes ist erzwungen, mit einer Neigung zur Seite. Die Krankheit geht oft in eine eitrige Mediastinitis über. 35. Behandlung und Prognose der akuten Ösophagitis Behandlung. Prinzipien der Behandlung der akuten Ösophagitis: ätiotrop, pathogenetisch und symptomatisch. Ätiotrope Behandlung - Behandlung der Grunderkrankung. Bei Infektionskrankheiten, die durch eine akute Ösophagitis kompliziert werden, werden Antibiotika (parenteral) eingesetzt. Bei ausgeprägten nekrotischen und hämorrhagischen Veränderungen der Speiseröhre wird empfohlen, für 2-3 Wochen auf Nahrung zu verzichten. Während dieser Zeit sind eine parenterale Ernährung, die intravenöse Verabreichung von Proteinhydrolysaten, Mischungen von Aminosäuren, Intralipid, Vitaminen und eine Entgiftungstherapie indiziert. Nach der Reduzierung der Entzündung werden thermisch und chemisch schonende Lebensmittel verordnet: warme Milch, Sahne, Gemüsesuppen, flüssige Cerealien. Um lokale Entzündungssymptome zu reduzieren - in Lösungen von Tannin 1%, Collargol - 2%, Novocain - 1-2% vor den Mahlzeiten. Adstringenzien werden in horizontaler Position mit tief abgesenktem Kopfende des Bettes eingenommen. In Ermangelung der Wirkung der lokalen Verabreichung von adstringierenden Präparaten werden nicht-narkotische Analgetika parenteral verschrieben. Um die Auswirkungen der Ösophagusdyskinesie zu reduzieren, werden prokinetische Medikamente (Cerucal, Raglan, Cisaprid) oral vor den Mahlzeiten verwendet. Bei mehreren Erosionen sind Wismutpräparate (Denol, Vikair) und Solcoseryl-Injektionen angezeigt. Bei hämorrhagischer Ösophagitis, kompliziert durch Blutungen, werden Aminocapronsäurepräparate, Vikasol, Dicynon verwendet. Bei massiven Blutungen wird eine Blut- oder Plasmatransfusion verordnet. Bei einer eitrigen, nekrotischen Ösophagitis sollte der Patient lange parenteral ernährt, eine massive Therapie mit mehreren Antibiotika eingesetzt und der Abszess entleert werden. Ösophagusstrikturen werden durch Bougierung korrigiert. In seltenen Fällen wird eine Gastrostomie angelegt. Vorhersage. Die Prognose der katarrhalischen und erosiven Ösophagitis ist günstig. Ein spontanes Verschwinden der Symptome einer Ösophagitis ist möglich, sofern die zugrunde liegende Erkrankung angemessen korrigiert wird. Die Prognose der pseudomembranösen, exfoliativen, phlegmonösen Ösophagitis ist ernst. In allen Fällen endet die Ösophagitis vorbehaltlich der Genesung von der Grunderkrankung mit der Bildung von Narbenstrikturen, die einer weiteren Korrektur bedürfen. Patienten mit schweren Formen der Ösophagitis, die durch Strikturen der Speiseröhre kompliziert sind, sind arbeitsunfähig. Die Prävention einer akuten Ösophagitis besteht in einer angemessenen und rechtzeitigen Diagnose und Behandlung der Grunderkrankung. 36. Ätiologie, Pathogenese, Krankheitsbild der chronischen Ösophagitis Chronische Ösophagitis ist eine bis zu 6 Monate andauernde chronische Entzündung der Schleimhaut der Speiseröhre. Die häufigste Variante ist die Magen-Darm-Ösophagitis (Refluxösophagitis), die durch ein Magengeschwür der Speiseröhre erschwert werden kann. Ätiologie und Pathogenese. Die Hauptursache der Krankheit ist der ständige Rückfluss von Mageninhalt in die Speiseröhre, manchmal Galle und Darminhalt, das heißt, peptische Ösophagitis ist eine aseptische Verbrennung der Speiseröhre durch Magensäure. Bei der Pathogenese der Refluxösophagitis sind das Aufstoßen von saurem Inhalt und eine Verletzung der Reinigung und Entleerung der Speiseröhre von Bedeutung. Es gibt fünf Kriterien für die Pathogenität von Reflux bei der Genese der peptischen Ösophagitis: Häufigkeit, Volumen, Aufstoßen, chemische Zusammensetzung, Zustand der Speiseröhrenschleimhaut und Empfindlichkeit gegenüber einem chemischen Faktor (Entzündung der Wände verringert die Empfindlichkeit), Entleerungsrate (Clearance) , die hauptsächlich von aktiver Peristaltik, alkalisierendem Speichel und Schleim abhängt. Begünstigt wird das Auftreten einer Refluxösophagitis durch Hernien der ösophagealen Zwerchfellöffnung, Zwölffingerdarmgeschwür, postgastrische Resektionsstörungen und Allergien. Auch eine allergische Veranlagung spielt eine Rolle. Die morphologische Untersuchung von Patienten mit peptischer Ösophagitis zeigt Ödeme, Hyperämie der Schleimhaut, Infiltration der Submukosa des supradiaphragmatischen Segments der Speiseröhre. Krankheitsbild. Typische Anzeichen einer Refluxösophagitis sind Brennen hinter dem Brustbein, Sodbrennen, Aufstoßen, das sich im Liegen verschlimmert, Schluckbeschwerden und die positive Wirkung der Einnahme von Antazida. Nach dem Essen können Schmerzen hinter dem Brustbein auftreten, die Angina pectoris ähneln. Das Auftreten von Schmerzen bei Refluxösophagitis ist mit einer peptischen Reizung der Speiseröhrenwand und ihren Krämpfen beim Aufstoßen von saurem Mageninhalt sowie mit einer Verletzung der vorgefallenen Schleimhaut verbunden. Besonderheiten dieses Schmerzes: sein langer, brennender Charakter, Lokalisation im Xiphoid-Prozess, Bestrahlung entlang der Speiseröhre, seltener in der linken Brusthälfte, keine merkliche Wirkung durch Einnahme von Antazida, Antispasmodika, verstärkt in horizontaler Position, besonders danach Essen. Besondere Aufmerksamkeit sollte bei der klinischen Diagnose geringfügigen Symptomen einer Dysphagie geschenkt werden, wie z. B. dem Gefühl eines Knotens hinter dem Brustbein oder dem Gefühl, dass heiße Nahrung durch die Speiseröhre gelangt. Ein Zeichen für eine allmählich beginnende Ösophagitis kann Speichelfluss und die Gewohnheit sein, Wasser mit Nahrung zu trinken. Die körperliche Untersuchung von Patienten mit Refluxösophagitis liefert keine diagnostisch signifikanten Informationen. Zu den Komplikationen der Refluxösophagitis gehören Blutungen, Ulzerationen, Strikturen, Verkürzung der Speiseröhre und Malignität. Eine chronische Refluxösophagitis kann zur Entwicklung einer axialen Hiatushernie führen. 37. Diagnose, Behandlung der chronischen Ösophagitis Diagnose und Differentialdiagnose. Die wertvollste Forschungsmethode für diese Pathologie ist die Endoskopie, bei der Hyperämie, Ödeme und Verdickungen der Schleimhautfalten festgestellt werden. Es ist notwendig, eine Refluxösophagitis mit Magen- und Zwölffingerdarmgeschwür, koronarer Herzkrankheit, chronischer Cholezystitis und Pankreatitis zu differenzieren. Leitsymptom in der Differentialdiagnose ist der Schmerz. Die Differenzierung mit Magengeschwüren wird durch das Fehlen von späten und "hungrigen" Schmerzen bei Ösophagitis sowie durch Daten aus der Endoskopie der Speiseröhre und des Magens unterstützt. Der Koronarschmerz ist im Gegensatz zur Ösophagitis gekennzeichnet durch einen Zusammenhang mit körperlicher und seelischer Belastung, der Wirkung von Nitraten, Ischämiezeichen im EKG, auch solche nach Fahrradergometrie. Ultraschalldaten der Bauchorgane helfen, die Pathologie der Gallenblase und der Bauchspeicheldrüse als Ursache des Schmerzsyndroms auszuschließen. Behandlung. Die Therapie der Refluxösophagitis umfasst die Behandlung von Krankheiten, die sie verursacht haben, und die Ernennung einer Antirefluxtherapie. Den Patienten wird empfohlen, das Heben von Gewichten und das Bücken zu vermeiden. Während der Ruhe und des Schlafes muss die richtige Position eingenommen werden (das Kopfteil wird um 15-20 cm in einem Winkel von 30-50 angehoben). Es wird empfohlen, das Körpergewicht zu normalisieren, fraktioniert zu essen (die letzte Mahlzeit - 3 Stunden vor dem Schlafengehen). Alkohol und stark gewürzte Speisen sind von der Diät ausgeschlossen. Weisen Sie Adsorptionsmittel und alkalisierende Medikamente zu, die eine schützende Wirkung auf die Schleimhaut haben. Zu diesen Substanzen gehört Venter, das oral 1 g (vorzugsweise in Form einer Suspension) 30-40 Minuten vor den Mahlzeiten 3-mal täglich und das 4. Mal - auf nüchternen Magen vor dem Schlafengehen - verabreicht wird. Die Behandlungsdauer beträgt 8-10 Wochen. Almagel, Phosphalugel, Maalox, Gastal haben eine ähnliche Wirkung. Diese Medikamente werden in der Zwischenverdauungsperiode (1/2-2 Stunden nach den Mahlzeiten und nachts) verwendet, bis eine vollständige Remission eintritt. Phosphalugel und Maalox werden 1-2 Packungen 2-3 mal täglich verschrieben, gastal - 2-3 Tabletten pro Tag. Tea Soda, eine Mischung aus Bourget und weißer Tonerde, ist aufgrund unzureichender Effizienz nicht ratsam. Umhüllende und adstringierende Wirkung hat Wismutnitrat 1 g 3-4 mal täglich. Eine hohe Antirefluxaktivität eines neuen Antazidums, Topalkan, wurde festgestellt. Mineralwasser - "Borjomi", "Essentuki Nr. 4", "Jermuk", "Smirnovskaya" wirken alkalisierend. Um die saure Magensekretion zu reduzieren, werden Histamin-H2-Rezeptorblocker (Cimetidin, Ranitidin, Famotidin), Ka-K-ATPase-Inhibitoren (Omeprazol), ein selektiver Blocker der M-cholinergen Rezeptoren von Belegzellen und sein Analogon Buscopan verschrieben. Prognose und Prävention. Die Prognose für Leben und Arbeit ist günstig. Bei einem komplizierten Verlauf wird die Prognose durch die Aktualität und Qualität der medizinischen Versorgung bestimmt. Patienten mit schwerem Verlauf werden einer Behinderungsgruppe zugeordnet. Patienten mit chronischer Refluxösophagitis sollten unter der Aufsicht eines Gastroenterologen stehen. Mindestens 2-mal jährlich sind endoskopische und morphologische Untersuchungen aufgrund der Möglichkeit einer Malignität angezeigt. 38. Magengeschwür der Speiseröhre Magengeschwür der Speiseröhre ist eine akute oder chronische Erkrankung, die durch Ulzeration der Schleimhaut der distalen Speiseröhre unter dem Einfluss von aktivem Magensaft gekennzeichnet ist. Ätiologie und Pathogenese. Chronische Magengeschwüre der Speiseröhre sind Komplikationen der Refluxösophagitis und Hiatushernie. Ihr Auftreten wird durch die innere kurze Speiseröhre, fokale Metaplasie der Schleimhaut, Heterotopie der Magenschleimhaut in die Speiseröhre, Refluxkrankheit mit Kardiainsuffizienz, Erkrankungen mit häufigem Erbrechen (Post-Vagotomie-Syndrom, afferentes Schleifensyndrom, chronischer Alkoholismus) erleichtert. Krankheitsbild. Die Symptome eines Magengeschwürs der Speiseröhre ähneln dem Krankheitsbild einer peptischen Ösophagitis: anhaltendes Sodbrennen, Verschlimmerung nach dem Essen, beim Bücken, im Liegen, Aufstoßen, Schmerzen beim Schlucken und eingeschränkte Passage fester Nahrung. Die klinischen Symptome einer Perforation sind nicht von den Symptomen einer akuten penetrierenden und nicht penetrierenden mechanischen Verletzung durch Fremdkörper zu unterscheiden. Etwa 14 % der Speiseröhrengeschwüre dringen in das umgebende Gewebe ein. Diagnose und Differentialdiagnose. Aufgrund der klinischen Symptome ist es äußerst schwierig, ein Magengeschwür zu vermuten. Die Diagnose wird im Rahmen von Instrumental- und Laboruntersuchungen verifiziert. Die informativste Röntgen- und endoskopische Untersuchung. Die zuverlässigsten Informationen bei der Überprüfung von Magengeschwüren der Speiseröhre liefern Endoskopie und multiple Biopsie von den Rändern des Geschwürs. Beim Vorschieben des Endoskops zum Magengeschwür zeigen sich Anzeichen einer Ösophagitis im Stadium I-IV, einer motorischen Dysfunktion der Speiseröhre, eines perifokalen Ödems und einer Hyperämie der Schleimhaut. Es ist notwendig, Magengeschwüre der Speiseröhre mit Ulzerationen bestimmter Art (mit Tuberkulose, Syphilis) zu differenzieren. In diesen Situationen helfen spezifische serologische Tests, die Ergebnisse histologischer und bakteriologischer Studien erheblich. Die Kombination der Pathologie der Speiseröhre mit Schädigungen der Lunge und anderer Organe macht es erforderlich, den Patienten gezielt auf einen bestimmten Prozess hin zu untersuchen. Behandlung. Die Behandlung umfasst die Ernennung einer Diät: Es wird eine mechanisch und chemisch schonende Nahrung empfohlen, die 5-6 mal täglich in kleinen Portionen eingenommen wird. Um einen Rückfluss von Mageninhalt in die Speiseröhre zu verhindern, sollte die Bettlage des Patienten mit erhöhtem Kopfteil erfolgen. Medikamente werden im Liegen eingenommen. Weisen Sie eine Monotherapie mit einem Medikament einer der folgenden pharmakologischen Gruppen zu: antisekretorisch, einschließlich Antazida und Adsorbentien, Stimulanzien der motorischen Evakuierungsfunktion des Magens (Prokinetik), Medikamente - Schleimsimulatoren. Die Therapie wird lange durchgeführt - 1,5-3 Monate. Indikationen zur chirurgischen Behandlung - Ausbleibende Heilung innerhalb von 6-9 Monaten, komplizierter Verlauf (Perforation, Penetration, Stenose, Blutung). Prognose und Prävention. Die Prognose für Leben und Arbeit ist günstig. 39. Ätiologie, Pathogenese, Krankheitsbild der chronischen Gastritis Chronische Gastritis ist eine Krankheit, die klinisch durch Magendyspepsie und morphologisch durch entzündliche und degenerative Veränderungen der Magenschleimhaut, gestörte Zellerneuerungsprozesse und eine Zunahme der Anzahl von Plasmazellen und Lymphozyten in der schleimhauteigenen Membran gekennzeichnet ist. Ätiologie und Pathogenese. Auf dem gegenwärtigen Entwicklungsstand der Gastroenterologie wurde festgestellt, dass das Auftreten einer chronischen Gastritis durch die mikrobielle Ausbreitung von Helicobacter pylori (HP) gefördert wird, der in 95 % der Fälle eine antrale Gastritis und in 56 % der Fälle eine Pangastritis verursacht. Die ätiologischen Faktoren der chronischen Gastritis lassen sich mit hoher Sicherheit auf Risikofaktoren (unregelmäßige einseitige Ernährung, Rauchen, Alkoholkonsum, Hypersekretion von Salzsäure und Pepsin) zurückführen. Die führende Rolle bei der Entwicklung der Krankheit gehört auch zu Autoimmunmechanismen, begleitet von der Anhäufung von Antikörpern gegen die Belegzellen der Magenschleimhaut, einer verstärkten Vererbung sowie der Verwendung von Medikamenten, die eine schädigende Wirkung auf die Magenschleimhaut haben. Einstufung. 1990 wurde auf dem IX. Internationalen Kongress der Gastroenterologen in Australien eine neue Systematisierung der chronischen Gastritis angenommen, das so genannte Sydney-System. Histologische Grundlagen der Klassifikation. 1. Ätiologie: chronische Gastritis in Verbindung mit HP, autoimmune, idiopathische, akute arzneimittelinduzierte Gastritis. 2. Topographie: Antrum, Fundus, Pangastritis. 3. Morphologie: akute, chronische, Sonderformen. Endoskopische Klassifizierungsgrundlage: 1) Gastritis des Antrums des Magens; 2) Gastritis des Magenkörpers; 3) Pangastritis; 4) Veränderungen der Magenschleimhaut: Ödem, Erythem, Schleimhautanfälligkeit, Exsudat, flache Erosionen, erhabene Erosionen, Faltenhyperplasie, Faltenatrophie, Sichtbarkeit des Gefäßmusters, supramukosale Blutungen. Krankheitsbild. Chronische Gastritis ist eine der häufigsten Erkrankungen in der Klinik für innere Krankheiten. Seine Häufigkeit unter den Bewohnern der Erde reicht von 28 bis 75%. Chronische Gastritis äußert sich häufiger in Symptomen von Magendyspepsie und Schmerzen in der Magengegend. Selten ist es asymptomatisch. Ein ebenso wichtiger Platz im Krankheitsbild der chronischen Gastritis ist das dyspeptische Syndrom: Übelkeit, Aufstoßen (sauer, bitter, faul), Sodbrennen, Verstopfung oder Durchfall, instabiler Stuhl. Bei isolierter antraler Gastritis stehen Beschwerden über Sodbrennen und Verstopfung im Vordergrund, die durch die Hypersekretion von Salzsäure und Pepsin entstehen. 40. Diagnose und Behandlung von chronischer Gastritis Diagnose. Chronische Gastritis fließt lange, mit einer Zunahme der Symptome im Laufe der Zeit. Exazerbationen werden durch Ernährungsverletzungen provoziert. Das körperliche Bild einer chronischen Gastritis ist eher schlecht. Bei 80-90% der Patienten während einer Exazerbation der Krankheit bestimmt eine objektive Studie nur lokale Schmerzen in der Magengegend. Wenn chronische Gastritis mit Duodenitis, Cholezystitis oder Pankreatitis kombiniert wird, kann eine für Gastritis nicht typische, aber für die Pathologie eines anderen Organs charakteristische Schmerzlokalisation bestimmt werden. Eine Röntgenuntersuchung kann eher andere Erkrankungen des Magens (Geschwür, Krebs) ausschließen und bei der Diagnose von Morbus Menetrier helfen als die Diagnose einer chronischen Gastritis zu bestätigen. Aufgrund des Mangels an klinischen Manifestationen der Krankheit sowie der Unspezifität von Labortests basiert die Diagnose einer chronischen Gastritis auf den Ergebnissen endoskopischer und morphologischer Studien. Die Endoskopie zeigt Veränderungen in der Schwere der Magenschleimhaut unterschiedlicher Schwere: Ödem, Erythem, Vulnerabilität der Schleimhaut, Exsudat, flache Erosionen, erhabene Erosionen, Hyperplasie oder Atrophie der Falten, Sichtbarkeit des Gefäßmusters, submuköse Blutungen. Klinische Manifestationen, die für Gastritis charakteristisch sind, werden auch bei anderen Erkrankungen des Verdauungssystems beobachtet, daher sind im Diagnoseprozess Ultraschall der Bauchhöhle, eine gründliche endoskopische und morphologische Untersuchung der Verdauungsorgane erforderlich. Behandlung. Patienten mit Gastritis benötigen allgemeine medizinische Maßnahmen: regelmäßige ausgewogene Ernährung, Normalisierung des Arbeits- und Ruheregimes, Ausgleich von Stresssituationen zu Hause und am Arbeitsplatz. Медикаментозная терапия показана только при наличии клинических проявлений хронического гастрита. Больные с гастритом, ассоциированным с НР, лечатся по программе язвенной болезни (см. следующую лекцию). Лица с аутоиммунным гастритом нуждаются в назначении витамина В12 (по 500 мкг 1 раз в день подкожно в течение 30 дней с последующим повторением курсов лечения), фолиевой кислоты (по 5 мг в сутки), аскорбиновой кислоты (до 1 г в сутки). Bei Bedarf wird eine Ersatztherapie mit Enzympräparaten (Mezim-Forte, Festal, Enzistal, Kreon, Pancitrat, Acidin-Pepsin) durchgeführt. Das Schmerzsyndrom wird normalerweise durch die Ernennung von Antazida (Maalox, Almagel, Gastal) oder H-Histaminrezeptorblockern (Ranitidin, Famotidin) in mittleren therapeutischen Dosen gestoppt. Bei besonderen Formen der Gastritis ist eine Behandlung der Grunderkrankung notwendig. Prognose und Prävention. Die Prognose für Leben und Arbeit ist günstig. Die Vorbeugung von Gastritis wird auf eine rationelle Ernährung, die Einhaltung des Arbeits- und Ruheregimes und die Begrenzung der Einnahme von NSAIDs reduziert. 41. Ätiologie des Magengeschwürs Magengeschwür (Magengeschwür) ist eine chronische, rezidivierende Krankheit, die sich klinisch durch eine funktionelle Pathologie der gastroduodenalen Zone und morphologisch manifestiert - durch eine Verletzung der Integrität ihrer Schleim- und Submukosaschichten, und daher heilt das Geschwür immer mit der Bildung von eine Narbe. Ätiologie. Der wichtigste ätiologische Faktor von Magengeschwüren ist die mikrobielle Expansion von HP auf der Oberfläche des Magenepithels. Die Bedeutung der bakteriellen Aggression in der Ätiologie der Krankheit wurde seit 1983 untersucht, als J. Warren und B. Marshall über die Entdeckung einer großen Anzahl von S-Spiral-Bakterien auf der Oberfläche des Epithels des Antrums des Magens berichteten. Helicobakterien können aufgrund der Produktion des Urease-Enzyms, das Harnstoff (aus dem Blutkreislauf) in Ammoniak und Kohlendioxid umwandelt, in einer sauren Umgebung existieren. Die Produkte der enzymatischen Hydrolyse neutralisieren Salzsäure und schaffen Bedingungen für die Veränderung des pH-Werts der Umgebung um jede Bakterienzelle, wodurch günstige Bedingungen für die lebenswichtige Aktivität von Mikroorganismen geschaffen werden. Nicht weniger wichtig für die Entstehung von Magengeschwüren sind neuropsychische Effekte, erbliche Veranlagung, Infektionserreger, Ernährungsfehler und die Einnahme bestimmter Medikamente sowie schlechte Angewohnheiten. Erbliche Faktoren sind bei Forschern beliebt: Trägheit der wichtigsten Nervenprozesse, gruppenspezifische Eigenschaften des Blutes, immunologische und biochemische Merkmale, erbliches Belastungssyndrom. Beim Auftreten von Magengeschwüren wurde den Ernährungsstörungen eine wesentliche Bedeutung beigemessen. Klinische und experimentelle Studien, die in den letzten zwei Jahrzehnten durchgeführt wurden, zeigten jedoch in den meisten Fällen nicht die schädigende Wirkung von Nahrungsmitteln auf die gastroduodenale Schleimhaut. Die Prävalenz der peptischen Ulkuskrankheit unter erheblichen Kontingenten von Menschen mit unterschiedlichen Ernährungsgewohnheiten spricht ebenfalls gegen die führende Bedeutung von Ernährungsfaktoren. Störungen im Rhythmus und der Regelmäßigkeit der Ernährung, lange Pausen zwischen den Mahlzeiten, vorzeitiges Essen sind wesentlich für das Auftreten von Magengeschwüren. Forscher haben relativ widersprüchliche Ansichten über die Rolle von Alkohol bei der Ulkusentstehung geäußert. Es ist bekannt, dass Alkohol atrophische Veränderungen der Magenschleimhaut verursacht. Diese Beobachtungen stehen im Widerspruch zum allgemeinen Konzept der Ulzeration. Die Rolle medizinischer Wirkungen bei der Ulzerogenese wird aktiv untersucht. Die in der Literatur veröffentlichten Studienergebnisse und eigene Daten weisen darauf hin, dass nichtsteroidale Antirheumatika und Glukokortikoidhormone die ausgeprägtesten ulzerogenen Eigenschaften besitzen. 42. Diagnose von Magengeschwüren Diagnose. Im unkomplizierten Verlauf des Magengeschwürs gibt es keine Veränderungen im allgemeinen Bluttest, eine gewisse Abnahme der ESR, leichte Erythrozytose sind möglich. Mit dem Zusatz von Komplikationen tritt Anämie bei Blutuntersuchungen auf, Leukozytose - wenn das Peritoneum am pathologischen Prozess beteiligt ist. Es gibt keine Änderungen in der allgemeinen Analyse des Urins. Die traditionelle Untersuchungsmethode in der Pathologie des Magens ist die Bestimmung des Säuregehalts des Mageninhalts. Verschiedene Indikatoren sind möglich: erhöht und normal, in einigen Fällen sogar reduziert. Ein Zwölffingerdarmgeschwür tritt bei hohem Säuregehalt des Magensaftes auf. Bei der Röntgenuntersuchung ist ein Magengeschwür eine "Nische" - ein Depot von Bariumsuspension. Die Gastroduodenoskopie mit Biopsie ist die zuverlässigste Methode zur Diagnose von Magengeschwüren. Es ermöglicht Ihnen, die Art der Veränderungen der Schleimhaut am Rand des Geschwürs in der periulzerösen Zone zu beurteilen und garantiert die Genauigkeit der Diagnose auf morphologischer Ebene. In endoskopischen und morphologischen Studien wurde festgestellt, dass sich die meisten Magengeschwüre im Bereich der kleineren Krümmung und des Antrums befinden, viel seltener - auf der größeren Krümmung und im Bereich des Pyloruskanals. 90 % der Zwölffingerdarmgeschwüre befinden sich in der bulbären Region. Eine morphologische Untersuchung einer Biopsieprobe, die aus dem Boden und den Rändern des Geschwürs entnommen wurde, zeigt Zelldetritus in Form einer Schleimansammlung mit einer Beimischung von zerfallenden Leukozyten, Erythrozyten und abgestoßenen Epithelzellen mit darunter befindlichen Kollagenfasern. 43. Behandlung von Magengeschwüren Behandlung. Eine rationale Therapie bei Magengeschwüren sollte eine Kur, angemessene Ernährung, medikamentöse Behandlung, Psychotherapie, physikalische und Spa-Behandlungen umfassen. Während der Zeit der Verschlimmerung des Magengeschwürs ist es notwendig, die Fragmentierung der Ernährung genau zu beobachten (4 bis 6 mal täglich mit einer kleinen Menge jeder Portion Nahrung, die zu bestimmten Zeiten eingenommen wird). Lebensmittelprodukte sollten gute Puffereigenschaften haben und eine ausreichende Menge an Protein enthalten (120-140 g). Psychotherapie ist unerlässlich, um psychoneurotische Reaktionen zu stoppen oder zu reduzieren, die aus dem anhaltenden Schmerzsyndrom und seiner Erwartung resultieren. Arzneimittel zur Behandlung von Magengeschwüren werden in 5 Gruppen eingeteilt: 1) Medikamente, die den Säure-Peptic-Faktor beeinflussen (Antazida und Histamin-H2-Blocker, andere antisekretorische Mittel); 2) Medikamente, die die Barriere der Magenschleimhaut verbessern; 3) Medikamente, die die Synthese von endogenen Prostaglandinen erhöhen; 4) antibakterielle und antiseptische Mittel; 5) Medikamente, die motorische Evakuierungsstörungen des Magens und Zwölffingerdarms normalisieren. Antazida: 1) löslich (resorbierbar) - Natriumbicarbonat, Calciumcarbonat (Kreide) und Magnesiumoxid (gebrannte Magnesia); 2) unlöslich (nicht resorbierbar): Magnesiumtrisilikat und Aluminiumhydroxid. Mehrere Schemata der Kombinationstherapie (Zwei-, Drei-, Vierkomponenten). Zweikomponententherapie: Amoxicillin 1000 mg 2 mal täglich für 2 Wochen; Omeprazol 40 mg zweimal täglich. Das Drei-Komponenten-Schema umfasst die Zubereitung von kolloidalem Wismut 2 mg 120-mal täglich; Tetracyclin 4 mg 250-mal täglich; Metronidazol 4 mg 250-mal täglich. Der Therapiezyklus beträgt 4 Tage. Четырехкомпонентная схема предполагает омепразол по 20 мг 2 раза в сутки с 1-го по 10-й день; денол по 120 мг 4 раза в сутки с 4-го по 10-й день; тетрациклин по 500 мг 4 раза в сутки с 4-го по 10-й день; метронидазол по 500 мг 3 раза в сутки с 4-го по 10-й день. Наиболее эффективной признана четырехкомпонентная схема терапии язвенной болезни желудка и двенадцатиперстной кишки. Через 6 недель после ее проведения заживление пептического дефекта отмечается у 93-96 % больных. Nach Vernarbung eines Magen- und Zwölffingerdarmgeschwürs werden traditionell zwei Arten der Behandlung angewendet. 1. Eine kontinuierliche Erhaltungstherapie wird mit antisekretorischen Medikamenten in halber Tagesdosis über einen Zeitraum von bis zu einem Jahr durchgeführt. 2. Therapie „nach Bedarf“ beinhaltet die Anwendung eines der antisekretorischen Mittel in der halben Tagesdosis für zwei Wochen, wenn Symptome eines Magengeschwürs auftreten. 44. Chronische Enteritis. Ätiologie, Pathogenese, Klassifikation Chronische Enteritis ist eine Erkrankung des Dünndarms, gekennzeichnet durch eine Verletzung seiner Funktionen (Verdauung und Resorption) vor dem Hintergrund dystrophischer und dysregenerativer Veränderungen, die in der Entwicklung von Entzündungen, Atrophie und Sklerose der Schleimhaut des Dünndarms gipfeln. Ätiologie und Pathogenese. Dies ist eine polyätiologische Erkrankung, die das Ergebnis einer akuten Entzündung des Dünndarms oder eines primär chronischen Prozesses sein kann. Yersinia, Helicobacteria, Proteus, Pseudomonas aeruginosa, Rotaviren, zahlreiche Vertreter von Protozoen und Helminthen (Giardia, Ascaris, Bandwürmer, Opisthorchia, Cryptosporidium) haben in den letzten Jahren große Bedeutung als ätiologischer Faktor der chronischen Enteritis erhalten. Von großer Bedeutung für das Auftreten einer chronischen Enteritis sind Ernährungsfaktoren - übermäßiges Essen, Essen von Trockenfutter, unausgewogene, überwiegend kohlenhydrathaltige Lebensmittel, Missbrauch von Gewürzen. Enteritis wird durch ionisierende Strahlung, Exposition gegenüber toxischen Substanzen und Medikamenten verursacht. Zu den gemeinsamen pathogenetischen Mechanismen chronischer Erkrankungen des Dünndarms gehören Veränderungen der Darmflora vor dem Hintergrund einer Abnahme der lokalen und allgemeinen Immunität. Änderungen des Immunstatus - eine Abnahme des Gehalts an sekretorischem lgA, eine Erhöhung des lgE-Spiegels, eine Abnahme der Blastentransformation von Lymphozyten und eine Hemmung der Leukozytenmigration - führen zur Besiedlung des Dünndarms durch Vertreter der opportunistischen Mikroflora und a Abnahme der normalen anaeroben Flora. Morphologisch äußert sich die chronische Enteritis durch entzündliche und dysregenerative Veränderungen der Schleimhaut des Dünndarms. Wenn der Prozess fortschreitet, werden seine Atrophie und Sklerose beobachtet. Klassifizierung (Zlatkina A. R., Frolkis A. V., 1985). 1. Ätiologie: Darminfektionen, Helmintheninvasionen, alimentäre, physikalische und chemische Faktoren, Erkrankungen des Magens, der Bauchspeicheldrüse, der Gallenwege. 2. Krankheitsphasen: Exazerbation; Remission. 3. Schweregrad: leicht; mäßig; schwer. 4. Fluss: monoton; wiederkehrend; ständig wiederkehrend; latent. 5. Charakter der morphologischen Veränderungen: Einheit ohne Atrophie; Jeunitis mit mäßiger partieller Zottenatrophie; Jeunitis mit partieller Zottenatrophie; eunit mit totaler Zottenatrophie. 6. Die Art der Funktionsstörungen: Störungen der Membranverdauung (Disaccharidasemangel), Malabsorption von Wasser, Elektrolyten, Spurenelementen, Vitaminen, Proteinen, Fetten, Kohlenhydraten. 7. Komplikationen: Solaritis, unspezifische Mesadenitis. 45. Klinisches Bild und Diagnose einer chronischen Enteritis Krankheitsbild. Das Krankheitsbild der chronischen Enteritis besteht aus lokalen und allgemeinen enterischen Syndromen. Die erste ist auf eine Verletzung der Prozesse der parietalen (Membran) und Hohlraumverdauung (Maldigestion) zurückzuführen. Die Patienten klagen über Blähungen, Schmerzen in der paraumbilikalen Zone, Blähungen in Form einer Kappe, lautes Grollen, Durchfall, seltener Verstopfung. Die Palpation zeigt Schmerzen im Mesogastrium, sowie links und oberhalb des Nabels (positives Symptom von Porges), spritzendes Geräusch in der Gegend des Blinddarms (Symptom von Obraztsov). Kot erhält ein lehmiges Aussehen, Polyfäkalien sind charakteristisch. Das allgemeine enterale Syndrom ist mit einer gestörten Aufnahme von Nahrungsbestandteilen (Malabsorption) verbunden, was zu Störungen aller Arten des Stoffwechsels und Veränderungen der Homöostase führt. Gekennzeichnet durch vielfältige Stoffwechselstörungen, vor allem Eiweiß, die sich durch einen fortschreitenden Verlust des Körpergewichts äußern. Veränderungen im Kohlenhydratstoffwechsel sind weniger stark ausgeprägt, was sich durch Blähungen, Bauchgrummeln und vermehrtem Durchfall bei der Einnahme von Milchprodukten äußert. Der Mangel an Körpergewicht bei Patienten ist zu einem großen Teil nicht nur auf Protein, sondern auch auf ein Ungleichgewicht der Lipide zurückzuführen. Veränderungen im Fettstoffwechsel stehen in engem Zusammenhang mit Stoffwechselstörungen fettlöslicher Vitamine und Mineralstoffe (Kalzium, Magnesium, Phosphor). Die charakteristischen Anzeichen eines Kalziummangels sind ein positives Symptom der Muskelrolle, Krämpfe, wiederkehrende "unmotivierte" Knochenbrüche, Osteoporose, Osteomalazie. Diagnose und Differentialdiagnose. Ein allgemeiner Bluttest zeigt mikro- und makrozytäre Anämie, einen Anstieg der ESR und in schweren Fällen Lympho- und Eosinopenie. Wenn die Krankheit parasitären Ursprungs ist, können Lymphozytose und Eosinophilie im Blut beobachtet werden. Eine skatologische Untersuchung zeigt eine intestinale Art von Steatorrhoe aufgrund von Fettsäuren und Seifen, Creatorrhoe, Amylorrhoe. Der Gehalt an Enterokinase und alkalischer Phosphatase im Kot steigt an. Die tägliche Kotmasse nimmt deutlich zu. Ein biochemischer Bluttest zeigt Hypoproteinämie, Hypalbuminämie, Hypoglobulinämie, Hypokalzämie, verminderte Magnesium-, Phosphor- und andere Spurenelemente sowie Störungen des Elektrolytstoffwechsels in Form von verminderten Natrium- und Kaliumspiegeln. Das morphologische Bild einer milden Form der chronischen Enteritis ist gekennzeichnet durch Verdickung der Zotten, deren Verformung, Abnahme der Tiefe der Kerben, Abnahme des Tonus der glatten Muskulatur, subepitheliales Ödem, degenerative Veränderungen der Epitheloberfläche , Ausdünnung des Bürstensaums der Zellen, Abnahme der Anzahl der Becherzellen im Bereich der Zotten, Zunahme der Anzahl der Krypten, Infiltration der Schleimhaut der eigenen Schicht mit lymphoplasmatischen Elementen, Abnahme der Paneth-Zellen im Bereich von der Unterseite der Krypten. 46. Behandlung, Prognose der chronischen Enteritis Behandlung. Die Behandlung der chronischen Enteritis sollte umfassend sein, einschließlich Mitteln, die ätiologische Faktoren, pathogenetische Mechanismen sowie lokale und allgemeine Symptome der Krankheit beeinflussen. Grundlage ist die diätetische Ernährung, die hilft, den erhöhten osmotischen Druck in der Darmhöhle zu reduzieren, die Sekretion zu reduzieren und den Durchgang des Darminhalts zu normalisieren. Die medikamentöse Therapie sollte etiotrop, pathogenetisch und symptomatisch sein. Etiotrope Behandlung: Bei Dysbiose Grad II-IV werden antibakterielle Medikamente verschrieben: Metronidazol (0,5 g 3-mal täglich), Clindamycin (0,5 g 4-mal täglich), Cephalexin (0,5 g 2-mal täglich), Biseptol (). 0,48 g 2-mal täglich), Sulgin (1 g 3-4-mal täglich), Furazolidon (0,1 g 4-mal täglich). Nach der Einnahme von antibakteriellen Medikamenten werden Eubiotika verschrieben - Bifidumbacterin oder Bificol 5 Dosen 3-mal täglich 30 Minuten vor den Mahlzeiten, Colibacterin oder Lactobacterin 3 Dosen 3-mal täglich vor den Mahlzeiten, Hilak-Forte 40 Tropfen 3-mal täglich vor den Mahlzeiten. Die Behandlung mit Bakterienpräparaten wird über einen langen Zeitraum durchgeführt: 3 Zyklen à 3 Monate pro Jahr. Bei Staphylokokken-Dysbakteriose wird ein Antistaphylokokken-Bakteriophage verschrieben (20 ml 3-mal täglich für 15-20 Tage), bei Proteus-Dysbakteriose - Coliproteus-Bakteriophage oral, 20 ml 3-mal täglich, die Behandlungsdauer beträgt 2-3 Wochen. Zur Verbesserung des Verdauungsprozesses werden Enzyme empfohlen: Pankreatin, Panzinorm forte, Festal, Digestal, Pankurmen, Mezim forte, Trienzym, deren Dosierung individuell ausgewählt wird (von 1 Tablette 3-mal täglich bis 3-4 Tabletten 4-mal täglich ) und die direkt vor oder während der Mahlzeiten für 2-3 Monate verschrieben werden. Falls erforderlich, wird die Enzymersatztherapie über einen längeren Zeitraum fortgesetzt. Um Wasser- und Elektrolytstörungen zu korrigieren, sind intravenöse Verabreichung von Panangin 20-30 ml, Calciumgluconat 10% 10-20 ml in 200-400 ml isotonischer Lösung oder Glucoselösung, polyionische Lösungen "Disol", "Trisol", "Quartasol". angegeben. Elektrolytlösungen werden intravenös für 10-20 Tage unter Kontrolle des Säure-Basen-Zustands und des Blutelektrolytspiegels verabreicht. Prognose und Prävention. Die Prognose für das Leben und die Arbeitsfähigkeit ist in den meisten Fällen günstig. Prognostisch ungünstige Anzeichen sind ein kontinuierlich rezidivierender Krankheitsverlauf, ein starker signifikanter Gewichtsverlust, Anämie, ein Syndrom endokriner Störungen (verminderte Libido, Dysmenorrhoe, Unfruchtbarkeit). Die Prävention einer chronischen Enteritis besteht in der rechtzeitigen Behandlung akuter Darminfektionen und Begleiterkrankungen der gastroduodenalen Zone, in der Einhaltung der Diät, in der prophylaktischen Verabreichung von Bakterienpräparaten während der Röntgen- und Strahlentherapie. 47. Ätiologie, Pathogenese, Krankheitsbild von Morbus Crohn Morbus Crohn ist eine chronische Darmerkrankung mit systemischen Manifestationen; deren morphologische Grundlage eine granulomatöse Autoimmunentzündung des Magen-Darm-Traktes ist. Ätiologie und Pathogenese. Die Ätiologie und Pathogenese der Krankheit sind nicht gut verstanden. Am beliebtesten sind die Infektions- und Immunkonzepte des Ausbruchs der Krankheit. In den letzten Jahren gab es Berichte über die ätiologische Rolle von Mikroorganismen der Gattung Yersinia. Es ist jedoch schwierig festzustellen, ob es sich bei diesen mikrobiellen Agenzien um Krankheitserreger oder Kommensale handelt. Gleichzeitig spielen Veränderungen in der Darmflora eine wichtige Rolle in der Pathogenese der Erkrankung. Typischerweise eine Abnahme von Bakterien vom Bifidum-Typ bei gleichzeitiger Zunahme von Enterobakterien mit Anzeichen von Pathogenität. Autoimmunmechanismen spielen bei der Entstehung der Krankheit eine Rolle. Bei Morbus Crohn treten Autoantikörper (lgC, lgM) gegen Darmgewebe auf. Einstufung. Klassifizierung (F. I. Komarov, A. I. Kazanov, 1992). 1. Verlauf: akut; chronisch. 2. Merkmale des Prozesses: Läsion im Dünndarm; Läsion innerhalb der Ileozökalregion; Läsion innerhalb des Dickdarms. 3. Komplikationen: Verengung des Darms; toxische Erweiterung des Dickdarms; Fisteln; Amyloidose; Nephrolithiasis, Cholelithiasis; B12-Mangelanämie. Krankheitsbild. Das Krankheitsbild von Morbus Crohn ist durch eine erhebliche Vielfalt gekennzeichnet, die durch die Lokalisation und das Ausmaß des pathologischen Prozesses im Darm, die Form der Erkrankung und die Hinzufügung von Komplikationen bestimmt wird. Eine objektive Studie achtet auf die Blässe der Haut, die mit der Schwere der Anämie, Schwellungen in den Beinen aufgrund einer gestörten Resorption und des Proteinstoffwechsels korreliert. Beim Abtasten des Bauches werden Blähungen und Rumpeln festgestellt. Bei der körperlichen Untersuchung des Patienten werden Blässe der Haut, subfebriler Zustand, Körpergewichtsmangel festgestellt, Palpation zeigt krampfhafte Darmschlingen, Schmerzen in der paraumbilikalen Zone, in der rechten Iliakalregion. Bei Morbus Crohn werden extraintestinale Anzeichen der Krankheit festgestellt: aphthöse Stomatitis, Phlegmone und Fisteln der Mundhöhle, Arthritis, ähnlich der rheumatoiden Arthritis in der Klinik, mit charakteristischen Symptomen symmetrischer Läsionen kleiner Gelenke, Steifheit am Morgen. Typische Veränderungen am Auge: Iritis, Iridozyklitis, Makulopathie. Die Haut kann Erythema nodosa und Pyoderma gangraenosum entwickeln. Durchfall ist gekennzeichnet durch eine Zunahme der Stuhlhäufigkeit bis zu 10 Mal am Tag oder mehr, polyfäkale Materie. Das Volumen des Stuhls wird durch die anatomische Lokalisation des Prozesses bestimmt. Gewichtsverlust wird bei allen Patienten festgestellt. 48. Diagnose von Morbus Crohn Diagnose und Differentialdiagnose. Bei einem klinischen Bluttest während einer Exazerbation werden Leukozytose, Anämie und ein Anstieg der ESR festgestellt. Veränderungen in der allgemeinen Urinanalyse treten in schwerer Form auf, gekennzeichnet durch die Hinzufügung einer Amyloidose der Nieren (Proteinurie). Ein biochemischer Bluttest zeigt Hypoproteinämie, Hypoalbuminämie, einen Anstieg der a-Globuline, einen Rückgang des Gehalts an Eisen, Vitamin B12, Folsäure, Zink, Magnesium und Kalium. Die Daten der skatologischen Untersuchung erlauben eine indirekte Einschätzung der Läsionshöhe. Im Koprogramm mit Dünndarmlokalisierung des Prozesses werden polyfäkale Materie, Steatorrhoe, Creatorrhoe gefunden; mit dem Dickdarm - eine Beimischung von Schleim, Leukozyten, Erythrozyten. Mit der Röntgendiagnostik können Sie die Lokalisation und Prävalenz des pathologischen Prozesses im Darm feststellen. Bereiche des betroffenen Darms wechseln sich mit Bereichen des unveränderten Darms ab. Die veränderten Schlingen versteifen sich, das Bild ist mosaikartig mit kleinen Füllungsdefekten und mit dem Eindringen von Kontrastmittel über die Darmwand in Form von Taschen hinaus. Der Darm im betroffenen Bereich erhält den Charakter von fein gesäumten, mit der Bildung von Pseudodivertikeln. Die Kontraktionsfähigkeit der Darmwand wird reduziert oder geht ganz verloren, die Evakuierung von Barium verlangsamt sich. Es wird eine ungleichmäßige Verengung des Darmlumens beobachtet, wodurch es so eng wird, dass es die Form einer Spitze annimmt. Oberhalb der Verengungszone dehnt sich der Darm aus. Von entscheidender Bedeutung für die Diagnosesicherung ist die endoskopische Diagnostik. Am charakteristischsten für Morbus Crohn ist die Veränderung des Antrums des Magens und des Anfangsabschnitts des Zwölffingerdarms. Endoskopisch lässt sich eine kreisrunde Verengung des Antrums erkennen, die einer Tumorstenose ähnelt. Die Anfangsphase von Morbus Crohn ist durch schlechte endoskopische Daten gekennzeichnet: eine stumpfe Schleimhaut, an der Erosionen vom Typ Aphthen sichtbar sind, umgeben von weißlichen Granulationen. Das Gefäßmuster fehlt oder ist geglättet. Im Lumen des Darms und an seinen Wänden wird eitriger Schleim bestimmt. Bei klinischer Remission können die beschriebenen Veränderungen vollständig verschwinden. Mit fortschreitender Krankheit verdickt sich die Schleimhaut ungleichmäßig, hat eine weißliche Farbe und es werden große oberflächliche oder tiefe Risse festgestellt. Das Darmlumen verengt sich, was das Vorschieben des Koloskops erschwert. Die Koloskopie ermöglicht eine gezielte Biopsie der Schleimhaut in allen Teilen des Dickdarms und im terminalen Ileum. Bei Morbus Crohn beginnt der pathologische Prozess in der Submukosaschicht, daher sollte die Biopsie so durchgeführt werden, dass ein Teil der Submukosaschicht in das Biopsiematerial gelangt. Im Zusammenhang damit wird in 54% der Fälle das morphologische Substrat der Krankheit nicht erkannt. 49. Behandlung von Morbus Crohn Behandlung. Eine mechanisch und chemisch schonende Ernährung mit einem hohen Gehalt an Proteinen, Vitaminen, Spurenelementen ist vorgeschrieben, mit Ausnahme von Milch bei Unverträglichkeit und der Einschränkung von groben Pflanzenfasern. Die Verwendung von flüssigen enteralen Hydrolysaten wird gezeigt. Salazopräparate und Kortikosteroide bilden die Grundlage der pathogenetischen medikamentösen Therapie. Die tägliche Dosis von Medikamenten beträgt 3-6 g.Mit der Lokalisierung des pathologischen Prozesses im Dickdarm übersteigt die Aktivität von Sulfasalazin die Aktivität von Prednisolon. In Abwesenheit der Wirkung der Anwendung von Sulfasalazin, bei Läsionen überwiegend des Dünndarms und ausgeprägten Anzeichen einer Immunentzündung sowie bei Vorliegen systemischer Manifestationen der Krankheit ist die Anwendung von Kortikosteroiden angezeigt. Die Wirkung ihrer Anwendung wird in den ersten 8 Wochen nach Beginn der Behandlung festgestellt. Prednisolon wird nach folgendem Schema verschrieben: Auf dem Höhepunkt einer Exazerbation 60 mg pro Tag, dann wird die Dosis schrittweise reduziert und in der 6.-10. Woche auf eine Erhaltungsdosis von 5-10 mg pro Tag eingestellt. Bei Erreichen einer klinischen Remission wird das Medikament schrittweise abgesetzt. Wenn keine Remission erreicht wird, wird die Behandlung mit Prednisolon ambulant bis zur 52. Woche fortgesetzt. Bei schwerem Krankheitsverlauf, bei Komplikationen in Form von träge laufenden rektovaginalen, hautenteralen, enteroenteralen Fisteln, ist die Ernennung von 6-Mercaptopurin oral zu 0,05 g 2-3 mal täglich für 10 Tage angezeigt Kurse im Abstand von 3 Tagen bis zum Erreichen einer klinischen Remission. Anschließend wechseln sie zur Einnahme von Erhaltungsdosen des Medikaments im Laufe des Jahres. Die Dosis von 6-Mercaptopurin beträgt in diesem Fall 75 mg pro Tag. Die Wirkung der Behandlung mit Immunsuppressiva kann frühestens nach 3-4 Monaten festgestellt werden. Широкое применение в лечении болезни Крона нашел метронидазол, основными показаниями к назначению которого являются перианальные свищи и трещины, отсутствие эффекта от салазопрепаратов и глюкокортикоидов, а также рецидивы заболевания после проктэкто-мии. Препарат назначают в дозе 500-1000 мг в сутки. Продолжительность непрерывного курса не должна превышать 4 недель. Симптоматическая терапия болезни Крона сводится к назначению коротких курсов (по 2-3 дня) антидиарейных препаратов (имодиума, лоперамида). Дозы подбираются индивидуально по клиническому эффекту. Не следует назначать антидиарейные средства длительно (более 5 дней). В связи с наличием при болезни Крона синдрома мальабсорбции используют ферментные препараты, не содержащие желчных кислот (панкреатин, мезим-форте, солизим, сомилаза) в дозе от 2 до 6 таблеток с каждым приемом пищи. По показаниям проводится коррекция анемии и гипоальбуминемии назначением препаратов железа (парентерально) и введением альвезина, гидролизаторов белков, аминопептида, аминокровина. Назначают поливитамины в драже, эссенциале в капсулах. Лечение дисбактериоза проводят по общим правилам. 50. Klassifikation der unspezifischen Colitis ulcerosa Die unspezifische Colitis ulcerosa ist eine entzündliche Erkrankung der Dickdarmschleimhaut mit ulzerativ-destruktiven Veränderungen, die einen chronisch rezidivierenden Verlauf hat, oft begleitet von der Entwicklung lebensbedrohlicher Komplikationen. Klassifizierung (Yu. V. Baltaitis et al., 1986). Klinisches Merkmal. 1. Klinische Form: 1) akut; 2) chronisch. 2. Strom: 1) schnell fortschreitend; 2) kontinuierlich rezidivierend; 3) wiederkehrend; 4) latent. 3. Aktivitätsgrad: 1) Exazerbation; 2) Fading-Exazerbation; 3) Vergebung. 4. Schweregrad: 1) Licht; 2) moderat; 3) schwer. Anatomisches Merkmal. 1. Makroskopische Eigenschaft: 1) Proktitis: 2) Proktosigmoiditis; 3) Zwischensumme Läsion; 4) totale Niederlage. 2. Mikroskopische Eigenschaft: 1) das Vorherrschen destruktiver Entzündungsprozesse; 2) Reduzierung entzündlicher Prozesse mit Wiedergutmachungselementen; 3) Folgen des Entzündungsprozesses Komplikationen. 1. Lokal: 1) Darmblutung; 2) Perforation des Dickdarms; 3) Verengung des Dickdarms; 4) Pseudopolyposis; 5) sekundäre Darminfektion; 6) Verschwinden der Schleimhaut; 7) toxische Dilatation des Dickdarms; 8) Malignität. 2. Allgemeines: 1) funktioneller Hypokortizismus; 2) Sepsis; 3) systemische Manifestationen - Arthritis, Sakroiliitis, Hautläsionen, Iritis, Amyloidose, Phlebitis, sklerosierende Cholangitis, Leberdystrophie. 51. Klinisches Bild der Colitis ulcerosa Krankheitsbild. Die Klinik der Colitis ulcerosa ist polymorph und hängt von der Schwere des Verlaufs und der Schwere des Prozesses ab. Der Verlauf des häufiger als chronisch angesehenen Entzündungsprozesses nimmt in manchen Fällen einen akuten Charakter an. Das Ausmaß der Kolonläsion kann ebenfalls variieren. Für die unspezifische Colitis ulcerosa sind 3 Leitsymptome charakteristisch: die Freisetzung von scharlachrotem Blut beim Stuhlgang, gestörte Darmfunktion und Bauchschmerzen. Darmfunktionsstörungen äußern sich in Form von Beschwerden über wiederholt instabilen Stuhlgang, der Folge einer ausgedehnten Schädigung der Schleimhaut und einer verminderten Aufnahme von Wasser und Salzen ist. Am häufigsten tritt Durchfall bei schwerer Colitis ulcerosa auf. Durchfall ist jedoch kein zuverlässiger Indikator für die Schwere des Prozesses. Die Schwere des Durchfalls in Kombination mit dem Vorhandensein von rotem Blut im Stuhl ist von Bedeutung. Bei einer beträchtlichen Anzahl von Patienten mit Colitis ulcerosa finden sich periodisch Blut und Schleim auf der Oberfläche des gebildeten Stuhls, was oft fälschlicherweise als Manifestation von Hämorrhoiden angesehen wird. Der milde Verlauf der unspezifischen Colitis ulcerosa ist durch einen zufriedenstellenden Zustand der Patienten gekennzeichnet. Bauchschmerzen sind mäßig und kurzfristig. Der Stuhl wird bis zu 2-3 mal am Tag dekoriert, beschleunigt. Blut und Schleim finden sich im Stuhl. Der Prozess ist im Rektum und Sigma lokalisiert. Der klinische Verlauf ist rezidivierend. Die Wirkung der Behandlung mit Salazopräparaten ist zufriedenstellend. Rückfälle treten nicht öfter als 2 Mal im Jahr auf. Remissionen können lang sein (mehr als 2-3 Jahre). Der mittelschwere Krankheitsverlauf wird diagnostiziert, wenn der Patient Durchfall hat. Der Stuhl ist häufig (bis zu 6-8 Mal am Tag), in jeder Portion ist eine Beimischung von Blut und Schleim sichtbar. Krämpfe im Unterleib sind intensiver. Es gibt Wechselfieber mit einem Anstieg der Körpertemperatur bis zu 38 C, intensive allgemeine Schwäche. Es können auch extraintestinale Manifestationen der Krankheit auftreten (Arthritis, Uveitis, Erythema nodosum). Der Verlauf ist ständig wiederkehrend, die Wirkung von Salazopräparaten ist instabil, bei Exazerbationen werden Hormone verschrieben. Die schwere Form der Erkrankung ist durch einen akuten Beginn gekennzeichnet. Mit der Ausbreitung des pathologischen Prozesses tief in die Darmwand entwickelt sich schnell eine totale Läsion des Dickdarms. Der Zustand des Patienten verschlechtert sich rapide. Die Klinik ist gekennzeichnet durch einen plötzlichen Beginn, hohes Fieber, starken Durchfall bis zu 24 Mal am Tag, starke Darmblutungen und eine rasch zunehmende Dehydratation. Tachykardie tritt auf, der Blutdruck sinkt, extraintestinale Manifestationen einer unspezifischen Colitis ulcerosa nehmen zu. Eine konservative Behandlung ist nicht immer wirksam, und oft ist eine Notoperation erforderlich. 52. Diagnose der unspezifischen Colitis ulcerosa Diagnose und Differentialdiagnose. Bei klinischen Blutuntersuchungen mit einer milden Form der Erkrankung werden eine leichte neutrophile Leukozytose, ein Anstieg der ESR und rote Blutbilder nicht verändert. Mit zunehmender Schwere des Verlaufs und zunehmender Dauer der Exazerbation kommt es zu einer Anämie gemischter Genese (B12-Mangel und Eisenmangel) und die BSG nimmt zu. Bei der biochemischen Analyse von Blut in mittelschweren und schweren Formen werden Dysproteinämie, Hypoalbuminämie, Hypergammaglobulinämie, Elektrolytstörungen und Säure-Basen-Zustand festgestellt. Bei der allgemeinen Urinanalyse treten Veränderungen nur auf, wenn Komplikationen in Form eines nephrotischen Syndroms vor dem Hintergrund einer Amyloidose auftreten, wenn charakteristische Veränderungen in Urintests auftreten - Proteinurie, "totes" Harnsediment, es kommt auch zu einer Zunahme des Blutes und der Gehalt an Kreatinin, Harnstoff. Die Hauptrolle in der Diagnostik kommt der endoskopischen Untersuchung mit gezielter Biopsie zu, da bei der unspezifischen Colitis ulcerosa primär die Dickdarmschleimhaut betroffen ist. Am pathologischen Prozess ist immer das Rektum beteiligt, d. h. erosive und ulzerative Veränderungen werden bei der Endoskopie unmittelbar hinter dem Analsphinkter bei der Sigmoidoskopie nachgewiesen. Bei Colitis ulcerosa ist die Rektosigmoidbiegung aufgrund starker Spasmen nicht immer zu überwinden. Der Versuch, den Schlauch des Proktoskops zu halten, wird von starken Schmerzen begleitet. In dieser Situation sollte das Proktoskop nicht tiefer als 12-15 cm eingeführt werden. Das endoskopische Bild hängt von der Form der Erkrankung ab. Bei einer milden Form sind ödematöse, stumpfe Schleimhaut, dicke weißliche Schleimüberzüge an den Darmwänden und leichte Kontaktblutungen sichtbar. Das Gefäßmuster der Submukosaschicht wird nicht visuell bestimmt. Im mittelschweren Krankheitsverlauf zeigen sich Hyperämie und Ödeme der Schleimhaut, schwere Kontaktblutungen, Blutungen, Erosionen und unregelmäßig geformte Geschwüre, dicke Schleimschichten an den Darmwänden. Bei einem schweren Krankheitsverlauf wird die Schleimhaut des Dickdarms in erheblichem Umfang zerstört. Es finden sich eine körnige, blutende Innenfläche, ausgedehnte Ulzerationen mit fibrinösen Ablagerungen, Pseudopolypen unterschiedlicher Größe und Form, Eiter und Blut im Darmlumen. Kontraindikationen für die Koloskopie und die Sigmoidoskopie sind schwere Formen der Colitis ulcerosa im akuten Krankheitsstadium. Bei Vorliegen einer Epidemie von Darminfektionen lässt sich die Diagnose leicht stellen. Aber auch bei sporadischer Morbidität bei akuten Darminfektionen verläuft das Colitis-Syndrom ohne Schübe, während die Colitis ulcerosa einen rezidivierenden Verlauf hat. Die genauesten Methoden zur Identifizierung einer akuten Darminfektion umfassen bakteriologische und serologische. 53. Behandlung von unspezifischer Colitis ulcerosa Behandlung. Das Fehlen eines einzigen ätiologischen Faktors und die Komplexität der Pathogenese der unspezifischen Colitis ulcerosa erschweren die Behandlung dieser Krankheit. Es werden entzündungshemmende und antibakterielle Medikamente verwendet: Salazopyridazin, Sulfasalazin, Salazodimethoxin, Salofalk. Eingenommenes Sulfasalazin zerfällt unter Beteiligung der Darmflora zu 5-Aminosalicylsäure und Sulfapyridin. Nicht absorbiertes Sulfapyridin hemmt das Wachstum anaerober Mikroflora im Darm, einschließlich Clostridien und Bakterioiden. Und dank 5-Aminosalicylsäure verursacht das Medikament nicht nur Veränderungen in der Darmflora, sondern moduliert auch Immunantworten, blockiert die Mediatoren des Entzündungsprozesses. Das Medikament wird in einer Dosis von 2-6 g pro Tag für die gesamte Dauer der aktiven Entzündung verschrieben. Wenn das Colitis-Syndrom abklingt, wird die Sulfasalazin-Dosis schrittweise auf eine Erhaltungsdosis reduziert (durchschnittlich 1-1,5 Tabletten pro Tag). Bei schwerem Durchfallsyndrom bei Personen mit leichtem und mittelschwerem Krankheitsverlauf ist Sandostatin indiziert, das die Synthese von Magen-Darm-Hormonen und biogenen Aminen (vasoaktives intestinales Peptid, Gastrin, Serotonin) hemmt, deren Produktion bei Colitis ulcerosa und stark erhöht ist Morbus Crohn. Außerdem reduziert das Medikament die Sekretion und verbessert die Absorption im Darm, hemmt den viszeralen Blutfluss und verringert die Beweglichkeit. Bei der Anwendung von Sandostatin (innerhalb von 7 Tagen bei einer Dosis von 0,1 mg 2-mal subkutan) nimmt der Durchfall ab, der Tenesmus verschwindet praktisch und die Blutausscheidung mit Kot nimmt ab. Bei einer schweren Form der unspezifischen Colitis ulcerosa erfolgt die Behandlung vor dem Hintergrund der parenteralen Ernährung. Der Proteingehalt dieser Präparate sollte etwa 1,5-2,0 g/kg Körpergewicht betragen. Kortikosteroide, die parenteral verabreicht werden, sind eine pathogenetische Behandlung für eine schwere Form der Erkrankung: Am ersten Tag wird Prednison intravenös in Abständen von 12 Stunden (90-120 mg oder mehr) verabreicht, in den nächsten 5 Tagen - intramuskulär, Dosis schrittweise reduzieren. Mit positivem Effekt wechseln sie zu oralen Medikamenten (Prednisolon 40 mg pro Tag). Bei der mittelschweren Verlaufsform des unspezifischen Ulcus ulcerosa ist eine strenge Diät mit einer Einschränkung von Ballaststoffen, Milchprodukten und einem hohen Proteingehalt erforderlich. Prednisolon wird oral in einer Anfangsdosis von 20-40 mg pro Tag verabreicht. Die Behandlung kann mit Sulfasalazin und seinen Analoga ergänzt werden, die oral eingenommen oder in Microclysters und Zäpfchen in das Rektum verabreicht werden. Die Anfangsdosis von Sulfasalazin beträgt 1 g pro Tag, dann wird sie auf 4-6 g erhöht. Als zusätzliche Behandlungsmethode können Abkochungen von Kräutern mit entzündungshemmender und hämostatischer Wirkung (Wurzel, Brennnesselblätter, Flechten, Grauerlenzapfen, Süßholzwurzel) verwendet werden. In der Kräutermedizin können Sie häufig die Dosis von Salazopräparaten reduzieren und verlängern Remission. 54. Klinisches Bild der akuten Gromerulonephritis Die akute Glomerulonephritis (AGN) ist eine akute diffuse Nierenerkrankung infektiös-allergischer Natur, die in den Glomeruli lokalisiert ist. AGN kann eine unabhängige Krankheit (primär) oder sekundär als Teil einer anderen Krankheit sein, was das klinische Bild und die Diagnose der letzteren erschwert. AGN betrifft in der Regel junge und Männer mittleren Alters. Krankheitsbild. Das klinische Bild der Krankheit besteht aus den folgenden Syndromen. Harnsyndrom. 1. Proteinurie aufgrund des Durchgangs von Proteinmolekülen durch die Räume der Kapillarwand des Glomerulus, die während der Ablagerung von Immunkomplexen auf ihnen gebildet werden. Proteinurie ist von Natur aus selektiv, bei der überwiegend Albumine den glomerulären "Filter" passieren. 2. Hämaturie aufgrund der Beteiligung am pathologischen Prozess des Kapillarmesangiums und des interstitiellen Gewebes. Erythrozyten dringen durch kleinste Risse in der Basalmembran ein und verändern ihre Form. 3. Cylindrurie - Urinausscheidung von zylindrischen Zellen der Tubuli. Während dystrophischer Prozesse in den Tubuli der zerfallenen Zellen des Nierenepithels bilden sich körnige Zylinder, die aus einer dichten körnigen Masse bestehen; wachsartige Zylinder haben scharfe Konturen und eine homogene Struktur; hyaline Abgüsse sind proteinhaltige Formationen. Das hypertensive Syndrom wird beobachtet aufgrund von: 1) Natrium- und Wasserretention; 2) Aktivierung des Renin-Angiotensin-Aldosteron- und sympathoadrenalen Systems; 3) Abnahme der Funktion des Depressorsystems der Nieren. Das Ödemsyndrom ist mit folgenden Faktoren verbunden: 1) eine Abnahme der glomerulären Filtration aufgrund ihrer Niederlage; 2) eine Abnahme der Filtrationsladung von Natrium und eine Zunahme seiner Reabsorption; 3) Wassereinlagerungen aufgrund von Natriumeinlagerungen im Körper; 4) ein Anstieg des BCC; 5) sekundärer Hyperaldosteronismus; 6) eine Zunahme der Sekretion von ADH und eine Zunahme der Empfindlichkeit des distalen Nephrons dafür, was zu einer Flüssigkeitsretention führt; 7) eine Erhöhung der Permeabilität der Kapillarwände und die Freisetzung von Plasma in das Gewebe; 8) eine Abnahme des onkotischen Plasmadrucks mit massiver Proteinurie. 55. Diagnose einer akuten Gromerulonephritis Diagnose. In 100% der Fälle werden bei Urintests Proteinurie unterschiedlichen Schweregrades, Zylindrurie und, was für die Diagnose am wichtigsten ist, Hämaturie unterschiedlichen Schweregrades diagnostiziert - von Mikrohämaturie (bis zu 10 Erythrozyten pro Sichtfeld) bis Makrohämaturie (obwohl ziemlich selten). Bei Verdacht auf AGN ist es jedoch erforderlich, eine Reihe wiederholter Urintests durchzuführen oder einen Nechiporenko-Test (Bestimmung der Anzahl der gebildeten Elemente in 1 μl) durchzuführen, da Erythrozyten möglicherweise nicht in einer einzigen Urinportion nachgewiesen werden. Ein Bluttest zeigt akute Phasenindikatoren (erhöhte Fibrinogen- und a2-Globulinspiegel, C-reaktives Protein, beschleunigte ESR), die Anzahl der Leukozyten ändert sich wenig, mäßige Anämie. Bei einem unkomplizierten AGN-Verlauf ändert sich der Gehalt an stickstoffhaltigen Substanzen (Kreatinin, Indikan, Harnstoff) im Blut nicht. In der Anfangsphase der Krankheit wird eine Veränderung des Reberg-Tests beobachtet - eine Abnahme der glomerulären Filtration und eine Zunahme der tubulären Reabsorption, die sich mit der Genesung normalisiert. Eine Röntgenuntersuchung bei Patienten mit schwerer arterieller Hypertonie kann eine mäßige Zunahme des linken Ventrikels zeigen, die die gleiche Größe annimmt, wenn sich der Patient erholt. Es gibt 3 klinische Varianten von AGN. 1. Monosymptomatische Variante: geringe Beschwerden, Fehlen von Ödemen und arterieller Hypertonie, es besteht nur ein Harnsyndrom; die häufigste Variante des Krankheitsverlaufs (86 % der Fälle). 2. Nephrotische Variante: Ödeme, Oligurie sind ausgeprägt, es ist möglich, den Blutdruck auf relativ niedrige Zahlen zu erhöhen, es wird bei 8% der Patienten festgestellt. 3. Erweiterte Version: Arterielle Hypertonie, hohe Werte erreichend (180/100 mm Hg), mäßig ausgeprägtes Ödem, Kreislaufversagen, tritt in 6 % der Fälle auf. 56. Behandlung der akuten Gromerulonephritis Behandlung. Die Behandlung von AGN ist komplex und umfasst die folgenden Aktivitäten. 1. Modus. Bei Verdacht auf AGN oder unmittelbar nach Feststellung der Diagnose sollte der Patient sofort ins Krankenhaus eingeliefert werden. Strenge Bettruhe ist für ca. 2-4 Wochen bis zum Abklingen der Ödeme und Normalisierung des Blutdruckes einzuhalten. Das Liegenbleiben sorgt für eine gleichmäßige Erwärmung des Körpers, was zu einer Verringerung des Vasospasmus (daher zu einer Senkung des Blutdrucks) und zu einer Erhöhung der glomerulären Filtration und Diurese führt. Nach der Entlassung aus dem Krankenhaus ist eine Heimbehandlung für bis zu 4 Monate ab dem Datum des Ausbruchs der Krankheit indiziert, was die beste Vorbeugung gegen den Übergang von AGN in das chronische Stadium darstellt. 2. Ernährung. Abhängig von der Schwere der klinischen Symptome ist es sehr wichtig, Flüssigkeit und Natriumchlorid einzuschränken. Bei einer erweiterten und nephrotischen Form wird ein vollständiges Fasten für 1-2 Tage mit einer Flüssigkeitsaufnahme in einer Menge empfohlen, die der Diurese entspricht. Am 2-3. Tag wird der Verzehr von kaliumreichen Lebensmitteln (Reisbrei, Kartoffeln) gezeigt. Die Gesamtmenge an Wasser, die pro Tag getrunken wird, sollte gleich der für den Vortag zugeteilten Urinmenge plus 300-500 ml sein. Nach 3-4 Tagen wird der Patient auf eine Diät mit Proteinrestriktion (bis zu 60 g pro Tag) umgestellt, und die Gesamtsalzmenge beträgt nicht mehr als 3-5 g / Tag. Eine solche Diät wird bis zum Verschwinden aller extrarenalen Symptome und einer starken Verbesserung des Harnsediments empfohlen. 3. Die medikamentöse Therapie umfasst in erster Linie eine antibiotische Therapie, die jedoch nur durchgeführt werden sollte, wenn die infektiöse Natur der AGN gesichert ist (Erreger isoliert und seit Krankheitsbeginn nicht mehr als 3 Wochen vergangen). Üblicherweise verschriebenes Penicillin oder seine halbsynthetischen Analoga in üblichen Dosierungen. Das Vorhandensein offensichtlicher Herde einer chronischen Infektion (Tonsillitis, Sinusitis usw.) ist auch eine direkte Indikation für eine Antibiotikatherapie. Diuretika bei der Behandlung von AGN sind nur bei Flüssigkeitsretention, erhöhtem Blutdruck und dem Auftreten von Herzinsuffizienz indiziert. Das wirksamste Furosemid (40-80 mg), das bis zur Beseitigung von Ödemen und Bluthochdruck verwendet wird. Es besteht keine Notwendigkeit für eine langfristige Verschreibung dieser Medikamente, 3-4 Dosen sind ausreichend. Bei fehlendem Ödem, aber anhaltender Hypertonie oder bei unzureichender blutdrucksenkender Wirkung von Saluretika werden Antihypertensiva (Clophelin, Dopegyt) mit einer von der Persistenz der arteriellen Hypertonie abhängigen Anwendungsdauer verschrieben. Bei längerer Proteinurie wird Indomethacin oder Voltaren mit 75-150 mg pro Tag verschrieben (ohne Hypertonie und Oligurie). Die Prognose ist günstig, bei verlängerten Formen besteht jedoch die Möglichkeit, dass der Prozess chronisch wird. Die Prävention von AGN läuft auf eine wirksame Behandlung von Herdinfektionen und eine rationale Verhärtung hinaus. Um den Ausbruch der Krankheit nach der Impfung rechtzeitig zu erkennen, ist bei allen Patienten, die auf ARVI übertragen wurden, eine Untersuchung des Urins erforderlich.
▪ Zusammenfassung der Werke der russischen Literatur der ersten Hälfte des XNUMX. Jahrhunderts ▪ Grundlagen der Soziologie und Politikwissenschaft. Krippe
Alkoholgehalt von warmem Bier
07.05.2024 Hauptrisikofaktor für Spielsucht
07.05.2024 Verkehrslärm verzögert das Wachstum der Küken
06.05.2024
▪ Neuer Bildsensor für Autokameras ▪ Robuste Speicherkarten von Silicon Power ▪ Biologisch abbaubare Leiterplatten für die Elektronik ▪ Regenwürmer können Kunstdünger ersetzen
▪ Abschnitt der Website Grundlagen der Ersten Hilfe (OPMP). Artikelauswahl ▪ Artikel von Henri de Monterlant. Berühmte Aphorismen ▪ Artikel Arbeiten an Saitenguss-Setzmaschinen. Standardanweisung zum Arbeitsschutz ▪ Artikel Triac-Leistungsregler. Enzyklopädie der Funkelektronik und Elektrotechnik ▪ Artikel Antennenausrichtungsgerät. Enzyklopädie der Funkelektronik und Elektrotechnik
Startseite | Bibliothek | Artikel | Sitemap | Site-Überprüfungen www.diagramm.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese





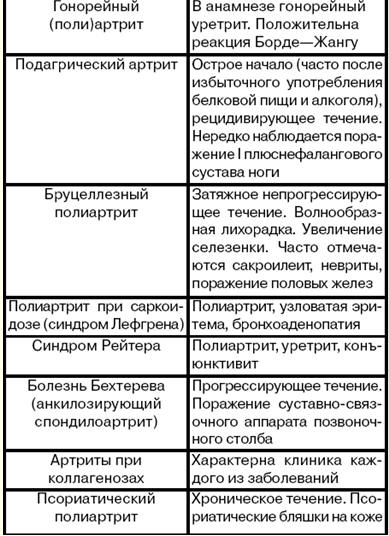
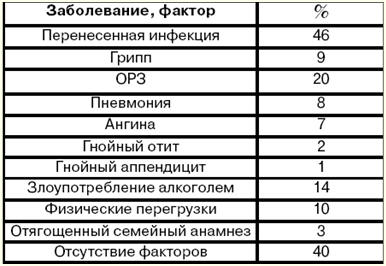
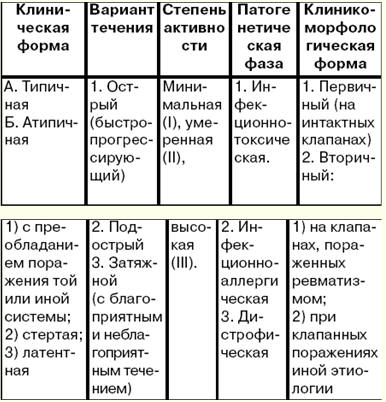
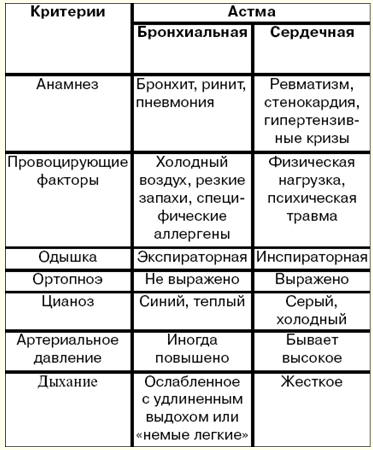

 Siehe andere Artikel Abschnitt
Siehe andere Artikel Abschnitt 